(2015·江苏,15改编)在体积均为1
0L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0
1molCO2和0
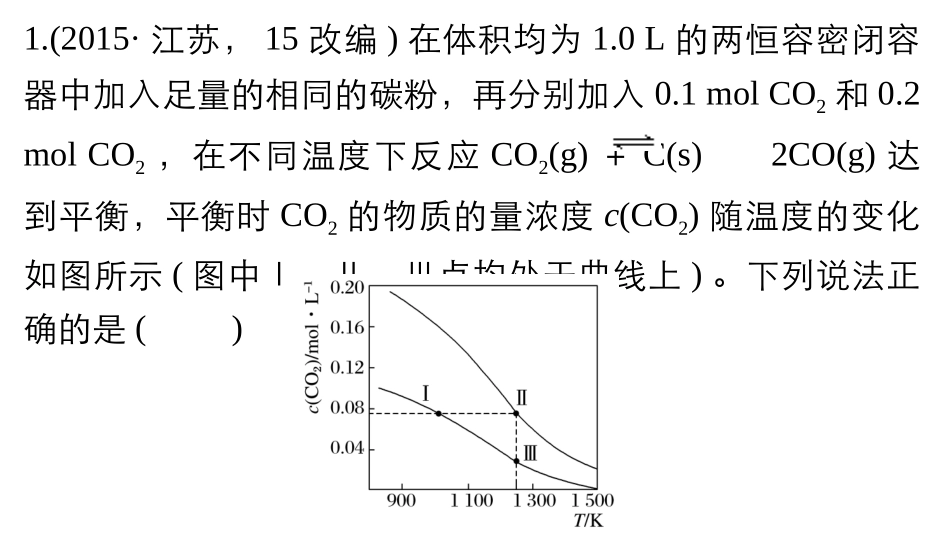
2molCO2,在不同温度下反应CO2(g)+C(s)2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)
下列说法正确的是()A
反应CO2(g)+C(s)===2CO(g)的ΔS>0、ΔH2p总(状态Ⅰ)C
体系中c(CO):c(CO,状态Ⅱ)>2c(CO,状态Ⅲ)D
逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ)解析A项,C和CO2反应是吸热反应,ΔH>0,故A错误;B项,状态Ⅰ是通入0
1molCO2,状态Ⅱ是通入0
2molCO2,状态Ⅱ可以看作先通0
1molCO2,此时的压强相等,再通入0
1molCO2,假如平衡不移动,此时的压强等于2倍p总(状态Ⅰ),但要满足CO2的浓度相等,应对此体系加热使反应向正反应方向移动,气体物质的量增加,因此p总(状态Ⅱ)>2p总(状态Ⅰ),故正确;C项,状态Ⅱ可以看作先通0
1molCO2,此时两者CO的浓度相等,再通入0
1molCO2,假如平衡不移动,状态ⅡCO的浓度等于2倍状态Ⅲ,但再充入CO2,相当于增大压强,平衡右移,消耗CO,因此c(CO,状态Ⅱ)