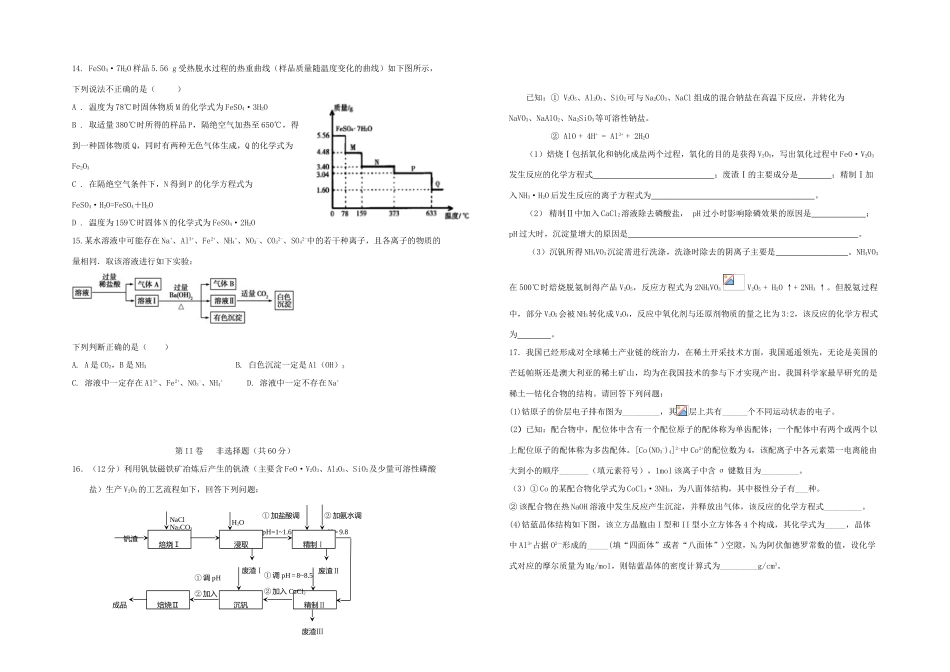
湖北省六校(恩施高中郧阳中学沙市中学十堰一中随州二中襄阳三中)2021届高三化学11月联考试题考试时间:90分钟试卷满分:100分可能用到的相对原子质量:C:12H:1O:16S:32Cl:35
5Cu:64Fe:56Cr:52第I卷选择题(共40分)一、选择题:本题共10小题,每小题2分,共20分
每小题只有一个选项符合题意
1.化学与生活密切相关
下列叙述错误的是A.宋·陈鼓年《广韵》中有“酢浆也,醋也”,食醋的主要成分为乙酸B.《抱朴子》中“丹砂(HgS)烧之成水银,积变又还成丹砂”,描述的是升华和凝华过程C.食盐中抗结剂K4[Fe(CN)6]中的铁元素显+2价D.ClO2和氯气均可作自来水的消毒剂2.2018年11月在法国凡尔赛召开了国际计量大会,会议将阿伏加德罗常数的定义修改为“1摩尔包含6
02214076×1023个基本单元,这一常数被称为阿伏加德罗常数,单位为mol-1”
若NA表示阿伏加德罗常数的值,则下列说法错误的是A.新定义中阿伏加德罗常数的不确定度被消除B.常温常压下,11
2LO2与N2组成的混合气体,含有原子个数小于NAC.117号元素符号为Ts(中文名),其重氢化物D293Ts含有中子数为177NAD.60
0gC3H8O中含有的C-C键可能小于2NA3.如图是硫元素在自然界中的循环示意图,下列有关说法不正确的是A.硫在自然界中既有游离态又有化合态B.过程⑤宜在土壤的富氧区实现C.硫元素的循环过程中既有硫的还原,又有硫的氧化D.若生物体有机硫的成键方式为,则过程④中S未发生氧化还原反应4
实验室中下列做法正确的是A.用煤油保存金属锂B.用水保存白磷C.用带有橡胶塞的棕色玻璃瓶保存浓硝酸D.用pH试纸测NaClO溶液的pH值5
已知NH4CuSO3与足量的10mol/L硫酸混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈