九年级化学酸、碱、盐(一)常见的酸、碱和盐【本讲主要内容】酸、碱、盐(一)——常见的酸、碱和盐常见的酸、碱、盐的物理性质,化学性质和用途
中和反应,溶液的酸碱度
【知识掌握】【知识点精析】一
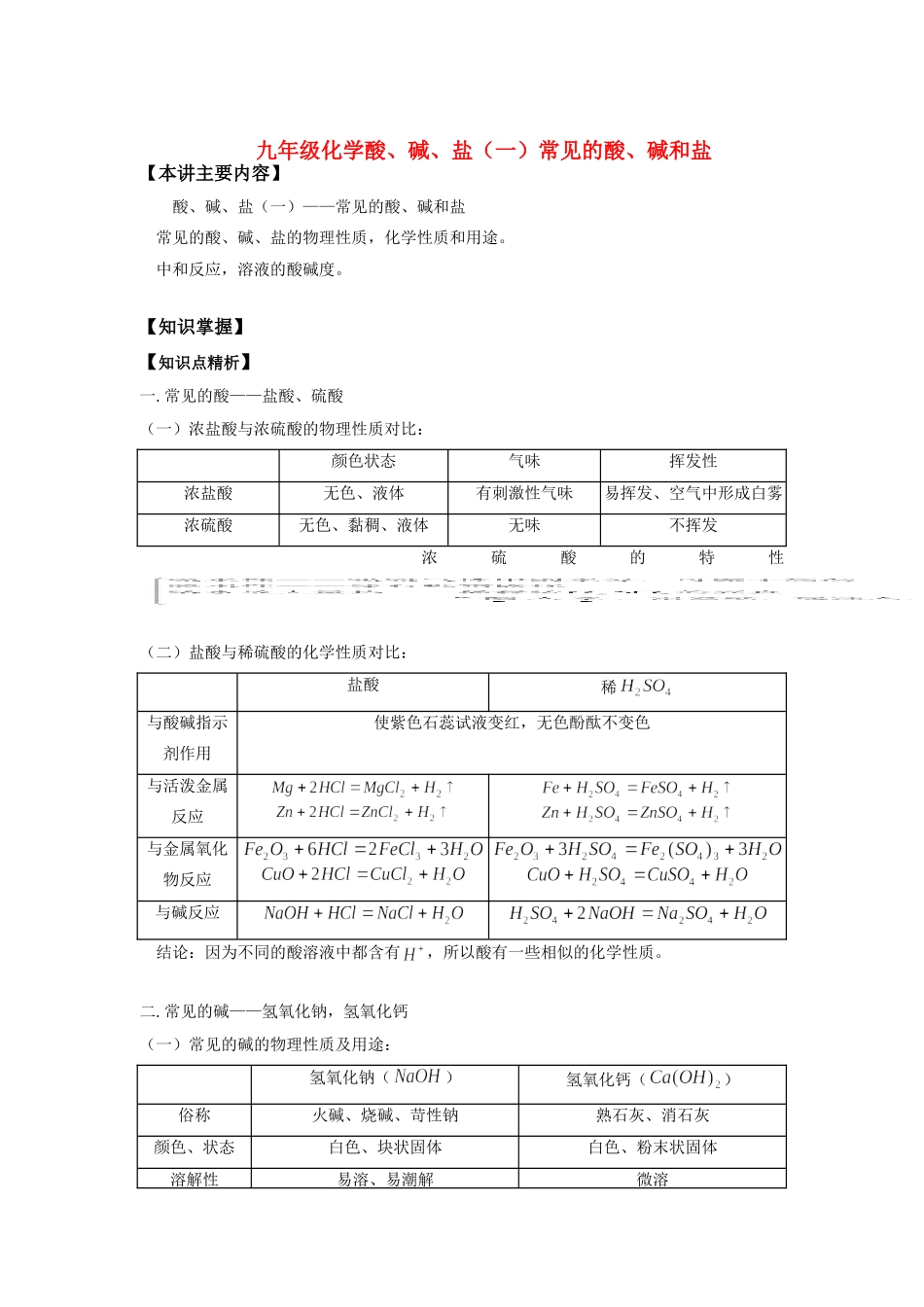
常见的酸——盐酸、硫酸(一)浓盐酸与浓硫酸的物理性质对比:颜色状态气味挥发性浓盐酸无色、液体有刺激性气味易挥发、空气中形成白雾浓硫酸无色、黏稠、液体无味不挥发浓硫酸的特性(二)盐酸与稀硫酸的化学性质对比:盐酸稀与酸碱指示剂作用使紫色石蕊试液变红,无色酚酞不变色与活泼金属反应与金属氧化物反应与碱反应结论:因为不同的酸溶液中都含有,所以酸有一些相似的化学性质
常见的碱——氢氧化钠,氢氧化钙(一)常见的碱的物理性质及用途:氢氧化钠()氢氧化钙()俗称火碱、烧碱、苛性钠熟石灰、消石灰颜色、状态白色、块状固体白色、粉末状固体溶解性易溶、易潮解微溶腐蚀性强腐蚀性较强腐蚀性用途重要化工原料,用于肥皂、石油、造纸、除油污重要建筑材料,工业原料,制漂白粉,改良土壤酸性等
(二)常见的碱的化学性质对比:氢氧化钠氢氧化钙与指示剂作用碱溶液使紫色石蕊试液变为蓝色,无色酚酞试液变为红色
与某些非金属氧化物反应与酸反应结论:因为不同的碱溶液中都含有,所以碱有一些相似的化学性质
中和反应:1
定义:酸和碱作用生成盐和水的反应
实质:酸溶液中的与碱溶液中的结合生成的过程
溶液的酸碱度——表示溶液酸碱性强弱程度的一种方法
pH与溶液酸碱性的关系2
pH的测定方法:将少量待测溶液滴在pH试纸上,将颜色与标准比色卡对照,读数
常见的盐盐——由金属离子和酸根离子组成的化合物
(一)常见的盐的性质对比(二)和的检验1
方法:样品石灰水变浑浊2
典型反应:【解题方法指导】例1
含有少量杂质的工业盐酸样品,经分析知只含,和,则杂质的化学式为_______,若测得溶液中与的个数比为20:1,则和的个数