九年级化学常见的碱及碱的通性、常见的盐及盐的性质知识精讲一
本周教学内容:常见的碱及碱的通性、常见的盐及盐的性质二
重点、难点:1
碱的分类和命名2
常见的碱的物理性质、化学性质、用途及其通性
盐的化学性质四
知识要点:1
碱的分类此外,碱也可分为强碱和弱碱,一元碱和二元碱等
碱的命名——“氢氧化某”——高价金属碱或“氢氧化亚某”——低价金属碱如:——氢氧化铁;——氢氧化亚铁——氢氧化铜;CuOH——氢氧化亚铜3
两种常见的碱的性质
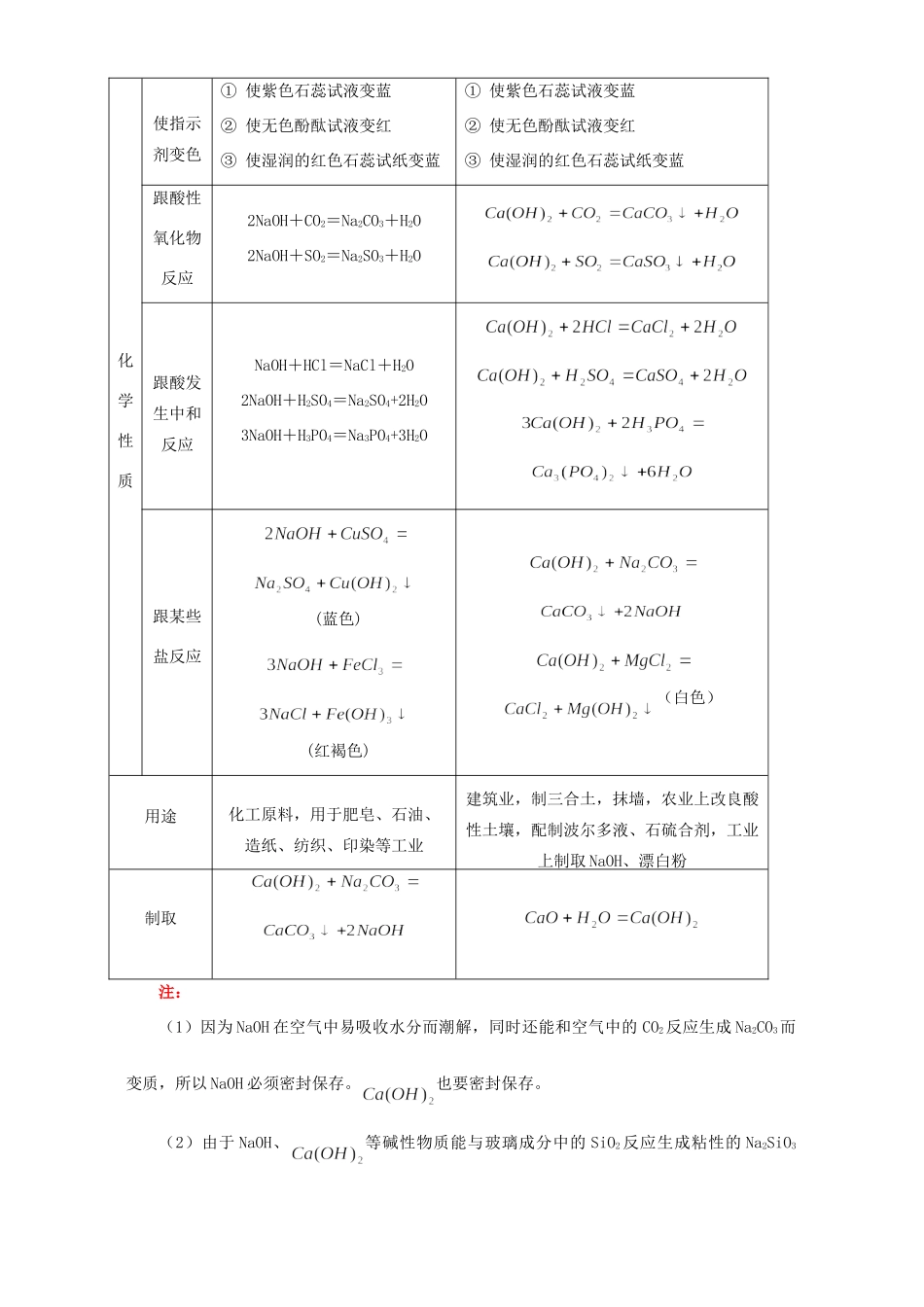
名称氢氧化钠氢氧化钙俗称火碱、烧碱、苛性钠熟石灰、消石灰(溶液为石灰水)化学式NaOHCa(OH)2相对分子质量4074电离方程式物理性等质色态白色固体白色粉末状固体吸湿性有强吸湿性,在空气中吸收水分,潮解无吸湿性(CaO有吸湿性)溶解性极易溶于水,强烈放热微溶于水,溶解度随温度升高而减小腐蚀性有强腐蚀性有强腐蚀性化学性质使指示剂变色①使紫色石蕊试液变蓝②使无色酚酞试液变红③使湿润的红色石蕊试纸变蓝①使紫色石蕊试液变蓝②使无色酚酞试液变红③使湿润的红色石蕊试纸变蓝跟酸性氧化物反应2NaOH+CO2=Na2CO3+H2O2NaOH+SO2=Na2SO3+H2O跟酸发生中和反应NaOH+HCl=NaCl+H2O2NaOH+H2SO4=Na2SO4+2H2O3NaOH+H3PO4=Na3PO4+3H2O跟某些盐反应(蓝色)(红褐色)(白色)用途化工原料,用于肥皂、石油、造纸、纺织、印染等工业建筑业,制三合土,抹墙,农业上改良酸性土壤,配制波尔多液、石硫合剂,工业上制取NaOH、漂白粉制取注:(1)因为NaOH在空气中易吸收水分而潮解,同时还能和空气中的CO2反应生成Na2CO3而变质,所以NaOH必须密封保存
也要密封保存
(2)由于NaOH、等碱性物质能与玻璃成分中的SiO2反应生成粘性的Na2SiO3(水玻璃)等物质使玻璃相互粘结,不易打