金属的化学性质课题铝与氢氧化钠溶液的反应物质的量在化学方程式计算中的应用总课时1班级(类型)学习目标1、掌握化学方程式中物质的量之比等于化学计量数之比重、难点1、物质的量在化学方程式计算中的应用学习环节和内容学生活动教师反思第二课时铝与氢氧化钠溶液的反应物质的量在化学方程式计算中的应用环节1新旧知识衔接-完成下列练习(1)铝和稀硫酸反应的离子方程式是2Al+6H+===2Al3++3H2↑,反应的还原剂是Al,氧化剂是H2SO4
(2)在标准状况下,46g钠和足量的水反应,则生成H2的质量为2_g,即2mol钠和足量的水反应,生成H2的物质的量为1mol,其体积为22
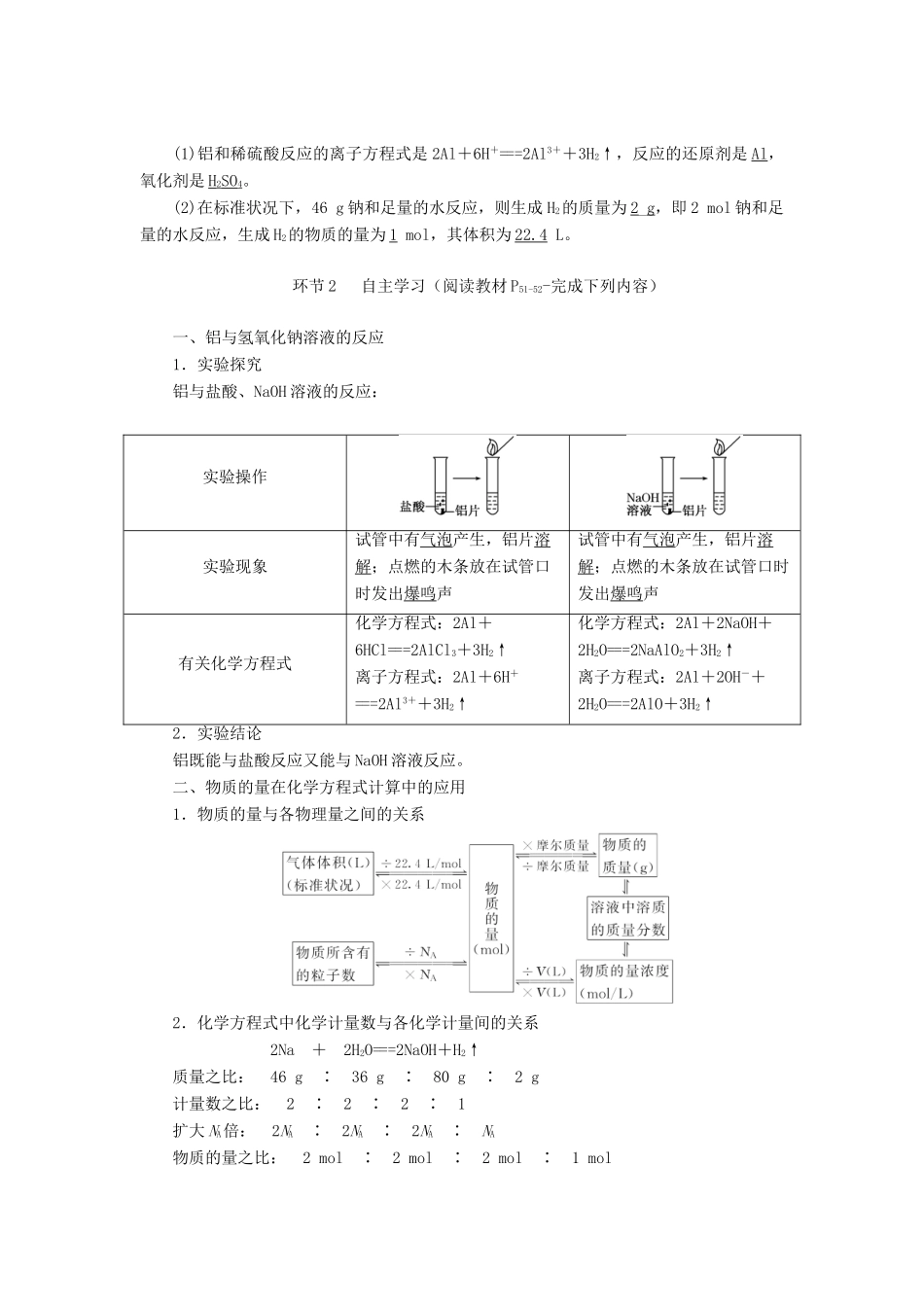
环节2自主学习(阅读教材P51-52-完成下列内容)一、铝与氢氧化钠溶液的反应1.实验探究铝与盐酸、NaOH溶液的反应:实验操作实验现象试管中有气泡产生,铝片溶解;点燃的木条放在试管口时发出爆鸣声试管中有气泡产生,铝片溶解;点燃的木条放在试管口时发出爆鸣声有关化学方程式化学方程式:2Al+6HCl===2AlCl3+3H2↑离子方程式:2Al+6H+===2Al3++3H2↑化学方程式:2Al+2NaOH+2H2O===2NaAlO2+3H2↑离子方程式:2Al+2OH-+2H2O===2AlO+3H2↑2.实验结论铝既能与盐酸反应又能与NaOH溶液反应
二、物质的量在化学方程式计算中的应用1.物质的量与各物理量之间的关系2.化学方程式中化学计量数与各化学计量间的关系2Na+2H2O===2NaOH+H2↑质量之比:46g∶36g∶80g∶2g计量数之比:2∶2∶2∶1扩大NA倍:2NA∶2NA∶2NA∶NA物质的量之比:2mol∶2mol∶2mol∶1mol结论:化学方程式中化学计量数之比等于粒子个数之比,也等于物质的量之比,对于有气体参与的反应还等于体积之比
环节3预习检测-发现问题1.铝制容器能否