氧化还原反应专题复习总结氧化还原反应是历年高考的重点和难点,高考命题的意图是考查对概念的理解,近几年来主要以选择题和填空题的形式来考查氧化还原反应的概念,并涉及物质结构、元素及其化合物的性质
如:1994年高考试题要求根据氧化还原反应方程式,判断元素的化合价,并确定其在元素周期表中的位置
[复习提示]1.氧化还原反应贯穿整个中学化学教材,既是重点又是难点
理解氧化还原反应的特征规律,掌握电子守恒原理的巧妙运用,同时明确基本概念,牢记常见氧化剂、还原剂性质的强弱顺序,即可顺利解题
2.近年常出现一些陌生而复杂的物质,给判断元素的化合价带来了困难,可这样处理:无机物运用正负化合价代数和为0的原则判断,有机物根据结构式判断
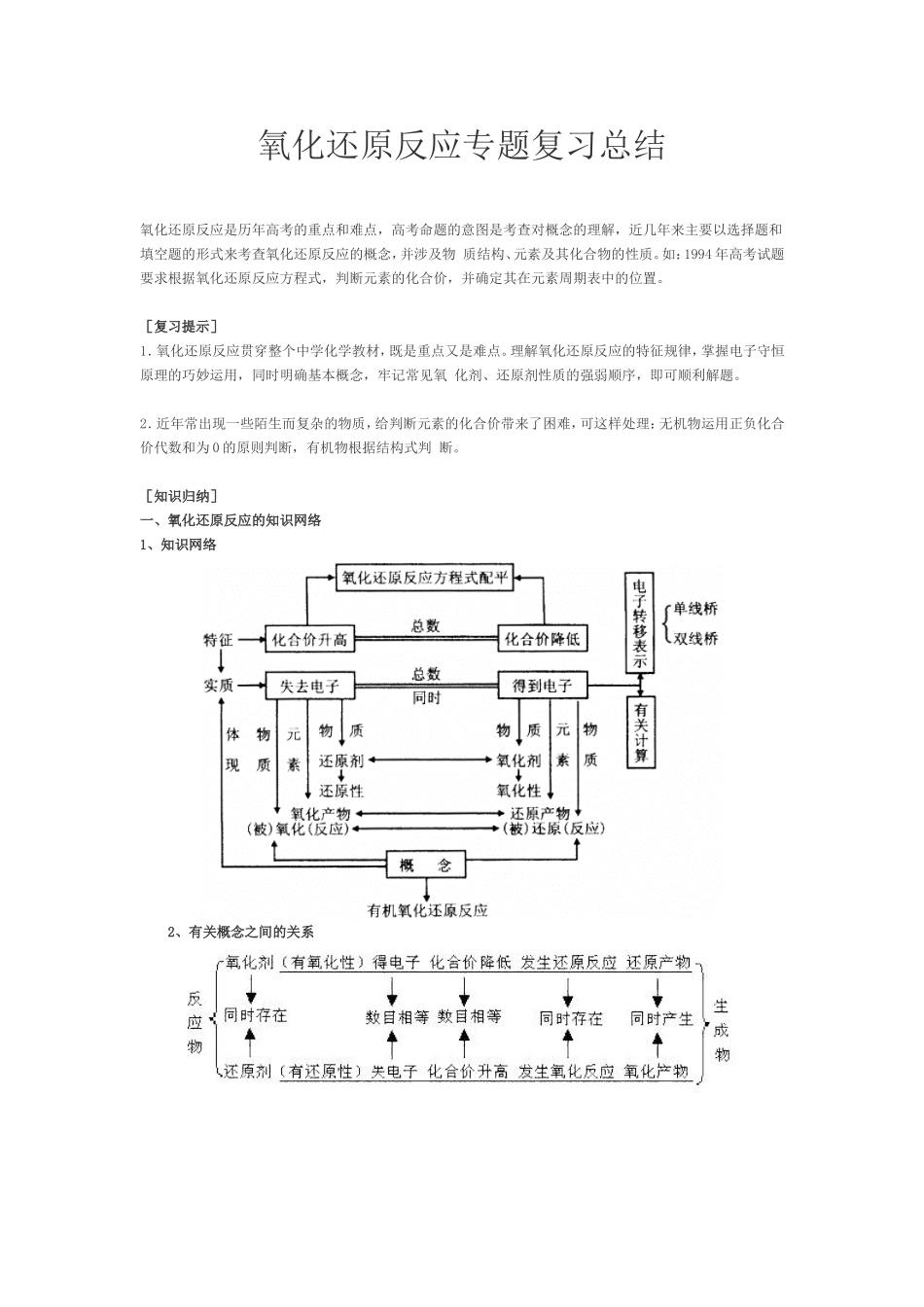
[知识归纳]一、氧化还原反应的知识网络1、知识网络2、有关概念之间的关系3、氧化性、还原性强弱比较4、常见的氧化剂和还原剂强氧化剂:KMnO4、K2Cr2O7、浓H2SO4、HNO3、Ca(ClO)2、H2O2、Na2O2、Cl2、Br2、O2等
强还原剂:活泼金属如Na、Mg、Al等,H2S、S2—、SO2、SO32—、H2SO3、I—、HI、Fe2+等
二、氧化还原反应方程式的配平及计算1.氧化还原方程式的配平原则(1)电子得失守恒:反应中还原剂失去电子总数(化合价升高总值)与氧化剂得到的电子总数(化合价降低总值)相等
(2)质量守恒:反应前后元素的种类相同,各元素的原子个数相等
2.氧化还原方程式的配平步骤一标:标明反应前后化合价有变化的元素前后化合价
二等:通过求最小公倍数使化合价升高与降低总值相等
三定:确定氧化剂与还原剂的化学计量数
方法是:氧化剂(还原剂)化学计量数=四平:用观察法配平其他物质的化学计量数
五查:检查质量与电荷是否分别守恒
3.氧化还原反应的有关计算其原理是:氧化剂得到的电子总数等于还原剂失去的电子总数
[例题分析]一、判断概念[