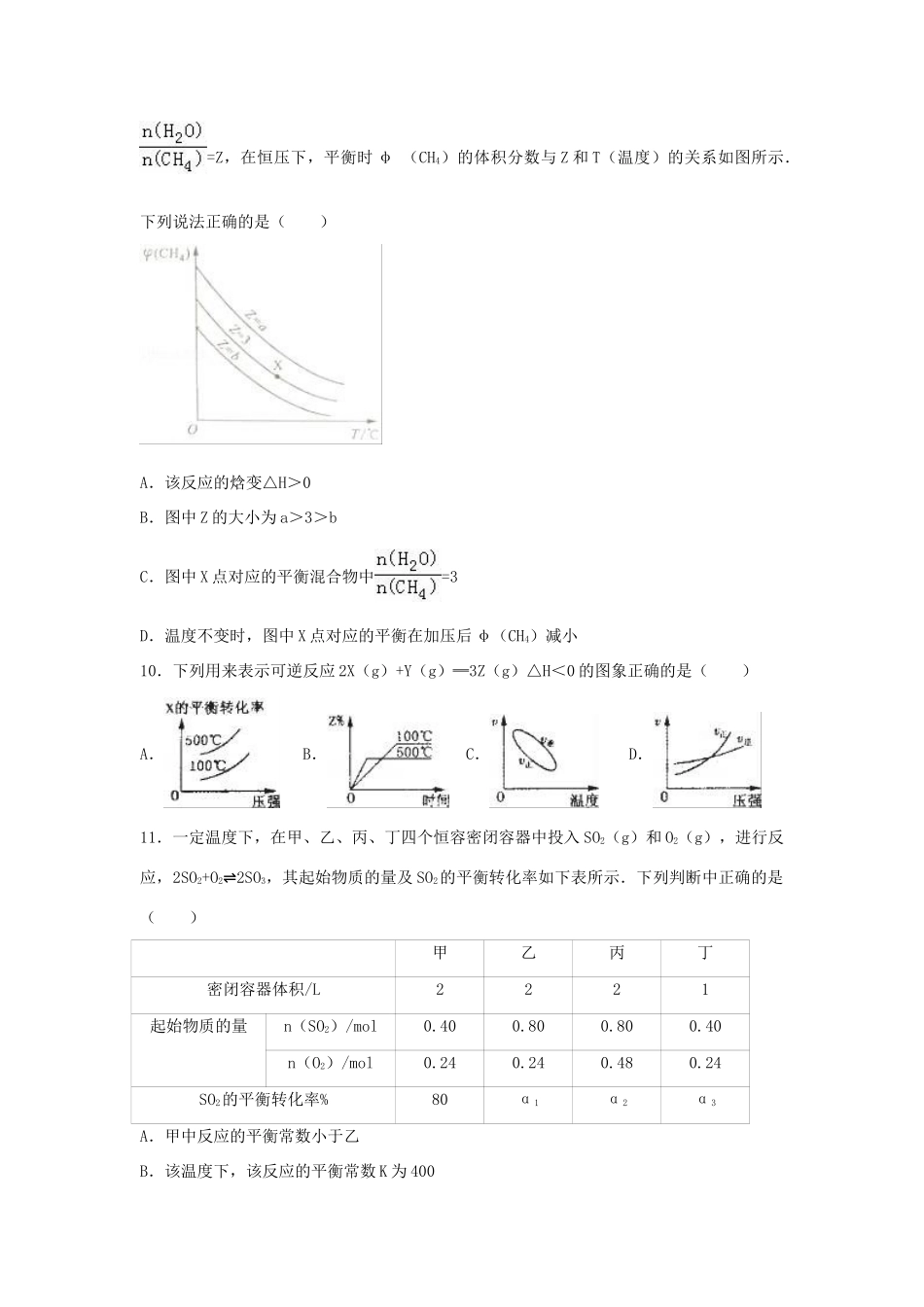
2016-2017学年河北省石家庄市高三(上)第三次月考化学试卷一、选择题(本大题共25小题,40分)1.下列物质加工或应用中未利用其化学性质的是()选项ABCD加工或应用油脂的硬化玉米酿酒石英传输光信号漂白精消毒A.AB.BC.CD.D2.设Na为阿伏加德罗常数的值.下列说法不正确的是()A.常温下,100g46%乙醇水溶液中含有H原子数为12NaB.23gNa与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NaC.标准状况下,2.24LCC14含有的共价鍵数为0.4NaD.lmolN2与4molH2反应生成的NH3分子数小于2Na3.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)⇌2HBr(g)△H<0,g平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b.a与b的关系是()A.a>bB.a=bC.a<bD.无法确定4.某离子反应中共有H2O、ClO﹣、NH4+、H+、N2、Cl﹣六种微粒.其中C(ClO﹣)随反应进行逐渐减小.下列判断错误的是()A.该反应的还原剂是NH4+B.消耗1mol氧化剂,转移2mol电子C.氧化剂与还原剂的物质的量之比是2:3D.反应后溶液酸性明显增强5.向含有0.2molFel2的溶液中加入amolBr2.下列叙述不正确的是()A.当a=0.1时,发生的反应为2I﹣+Br2═I2+2Br﹣B.当a=0.25时,发生的反应为2Fe2++4I﹣+3Br2═2Fe3++2I2+6Br﹣C.当溶液中I﹣有一半被氧化是,c(I﹣):c(Br﹣)═1:1D.当a=0.28时,4Fe2++10I﹣+7Br2═4Fe3++5I2+14Br﹣6.下列事实不能用勒夏特列原理解释的是()A.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深B.高压比常压有利于由SO2和氧气合成SO3的反应C.红棕色的NO2,加压后颜色先变深后变浅D.黄绿色的氯水光照后颜色变浅7.根据下图所给信息,得出的结论正确的是()A.碳的燃烧热为bkJ/molB.2C(s)+O2(g)═2CO(g)△H=﹣2(b﹣a)kJ/molC.2CO2(s)═2CO(g)+O2(g)△H=+akJ/molD.C(s)+O2(g)═CO2(g)△H<﹣bkJ/mol8.已知:H2S在高温下分解生成硫蒸气和H2.现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示,则生成的硫蒸气化学式为()A.SB.S2C.S6D.S89.一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)⇌CO(g)+3H2(g)设起始=Z,在恒压下,平衡时φ(CH4)的体积分数与Z和T(温度)的关系如图所示.下列说法正确的是()A.该反应的焓变△H>0B.图中Z的大小为a>3>bC.图中X点对应的平衡混合物中=3D.温度不变时,图中X点对应的平衡在加压后φ(CH4)减小10.下列用来表示可逆反应2X(g)+Y(g)═3Z(g)△H<0的图象正确的是()A.B.C.D.11.一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,2SO2+O2⇌2SO3,其起始物质的量及SO2的平衡转化率如下表所示.下列判断中正确的是()甲乙丙丁密闭容器体积/L2221起始物质的量n(SO2)/mol0.400.800.800.40n(O2)/mol0.240.240.480.24SO2的平衡转化率%80α1α2α3A.甲中反应的平衡常数小于乙B.该温度下,该反应的平衡常数K为400C.SO2的平衡转化率:α1>α2=α3D.容器中SO3的物质的量浓度:丙=丁<甲12.W、X、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Z是非金属元素,W、X的最高价氧化物对应的水化物可以相互反应生成盐和水,向一定量的W的最高价氧化物对应的水化物溶液中逐滴加入XZ3溶液,生成的沉淀X(OH)3的质量随XZ3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是()A.d点对应的溶液中:K+、NH4+、C032﹣、I﹣B.c点对应的溶液中:Ag+、Ca2+、NO3﹣、Na+C.b点对应的溶液中:Na+、S2﹣、SO42﹣、Cl﹣D.a点对应的溶液中:Na+、K+、S042﹣、HCO3﹣13.某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)⇌2C(g)达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物的量浓度、反应速率分别随时间的变化如图所示:下列说法中正确的是()A.4min时反应第一次达到平衡B.15min时降低压强,20min时升高温度C.反应方程式中的x=1,正反应为吸热反应...