高一化学物质结构、元素周期律的综合提高【本讲主要内容】物质结构、元素周期律的综合提高复习掌握1
原子的组成及同位素的概念,包括:掌握原子序数、核电荷数、质子数、中子数、核外电子数以及质量数与质子数、中子数之间的相互关系
以第1、2、3周期的元素为例,了解原子核外电子排布规律
掌握元素周期律的实质,了解元素周期表(长式)的结构(周期、族)
以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系
理解离子键、共价键的涵义
理解极性键和非极性键的涵义
了解键的极性和分子的极性
了解分子间作用力
熟记并正确书写常见元素的名称、符号、离子符号
掌握电子式、原子结构示意图、结构式的表示方法
【知识掌握】【知识点精析】一
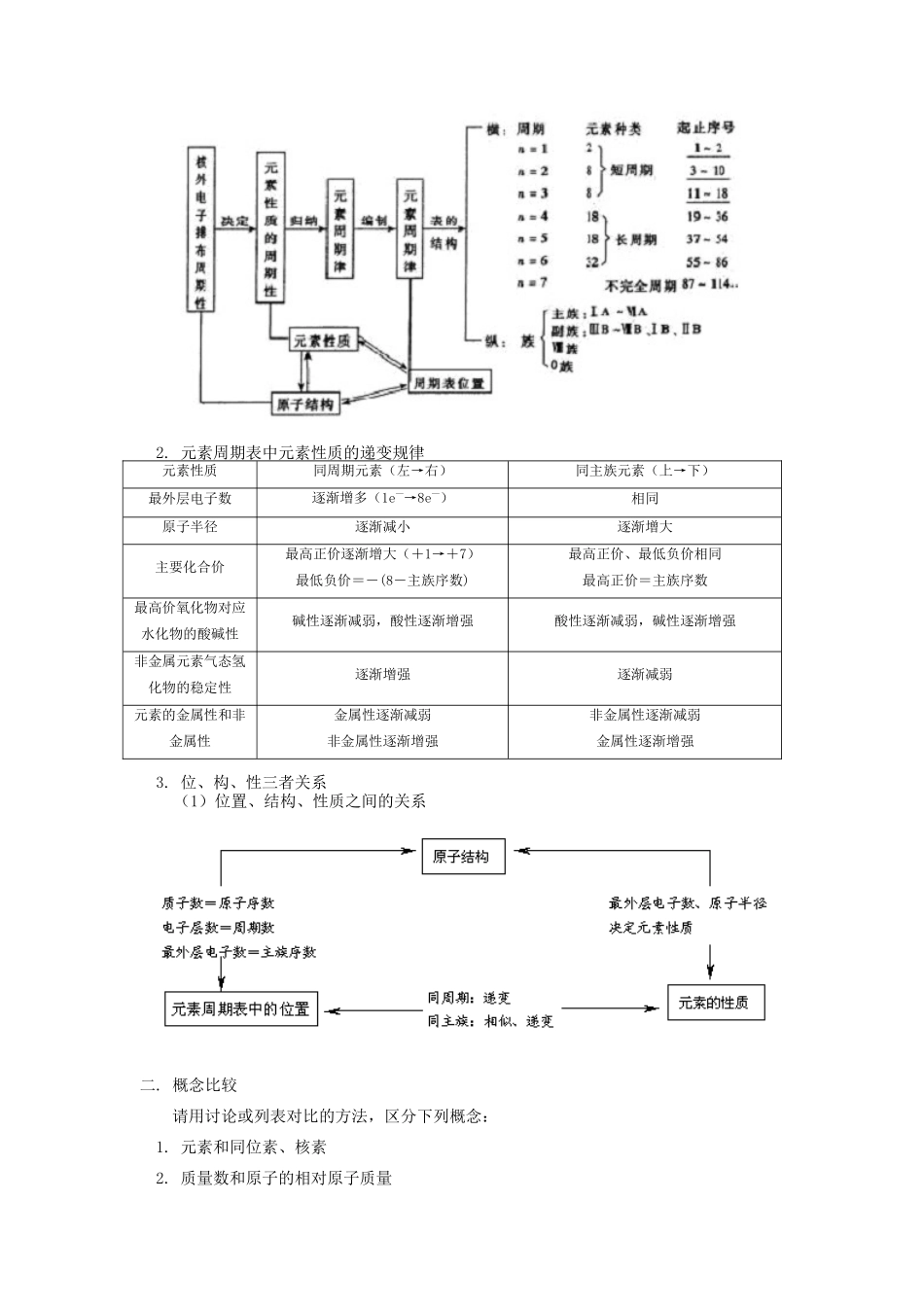
元素周期表中元素性质的递变规律元素性质同周期元素(左→右)同主族元素(上→下)最外层电子数逐渐增多(1e—→8e—)相同原子半径逐渐减小逐渐增大主要化合价最高正价逐渐增大(+1→+7)最低负价=-(8-主族序数)最高正价、最低负价相同最高正价=主族序数最高价氧化物对应水化物的酸碱性碱性逐渐减弱,酸性逐渐增强酸性逐渐减弱,碱性逐渐增强非金属元素气态氢化物的稳定性逐渐增强逐渐减弱元素的金属性和非金属性金属性逐渐减弱非金属性逐渐增强非金属性逐渐减弱金属性逐渐增强3
位、构、性三者关系(1)位置、结构、性质之间的关系二
概念比较请用讨论或列表对比的方法,区分下列概念:1
元素和同位素、核素2
质量数和原子的相对原子质量3
核外电子的运动特征和宏观物体的运动特征4
长周期和短周期;主族与副族5
元素的金属性和非金属性6
化合价与化学键7
离子键与共价键8
极性键与非极性键9
极性分子与非极性分子10
化学键的极性与分子的极性1