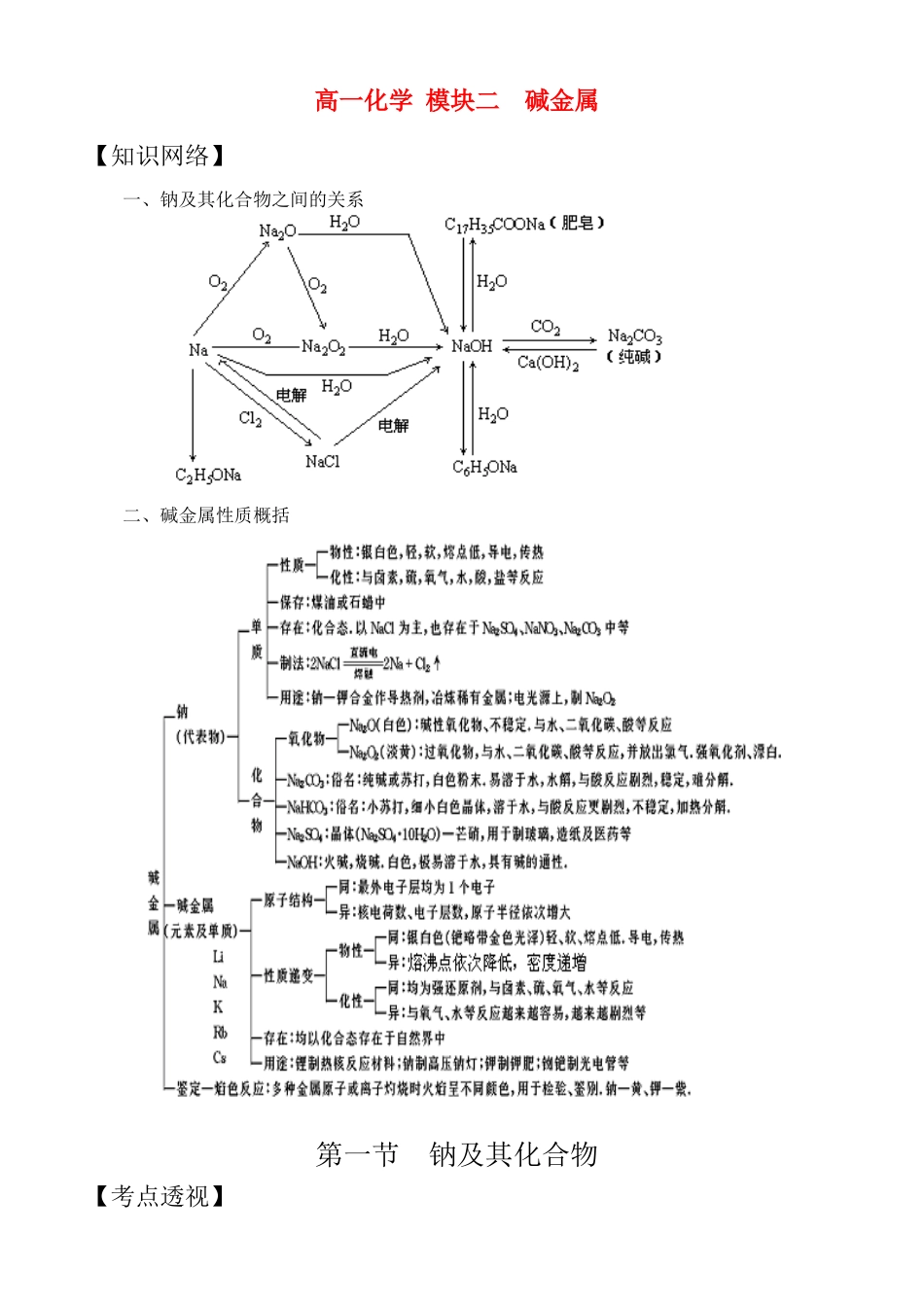
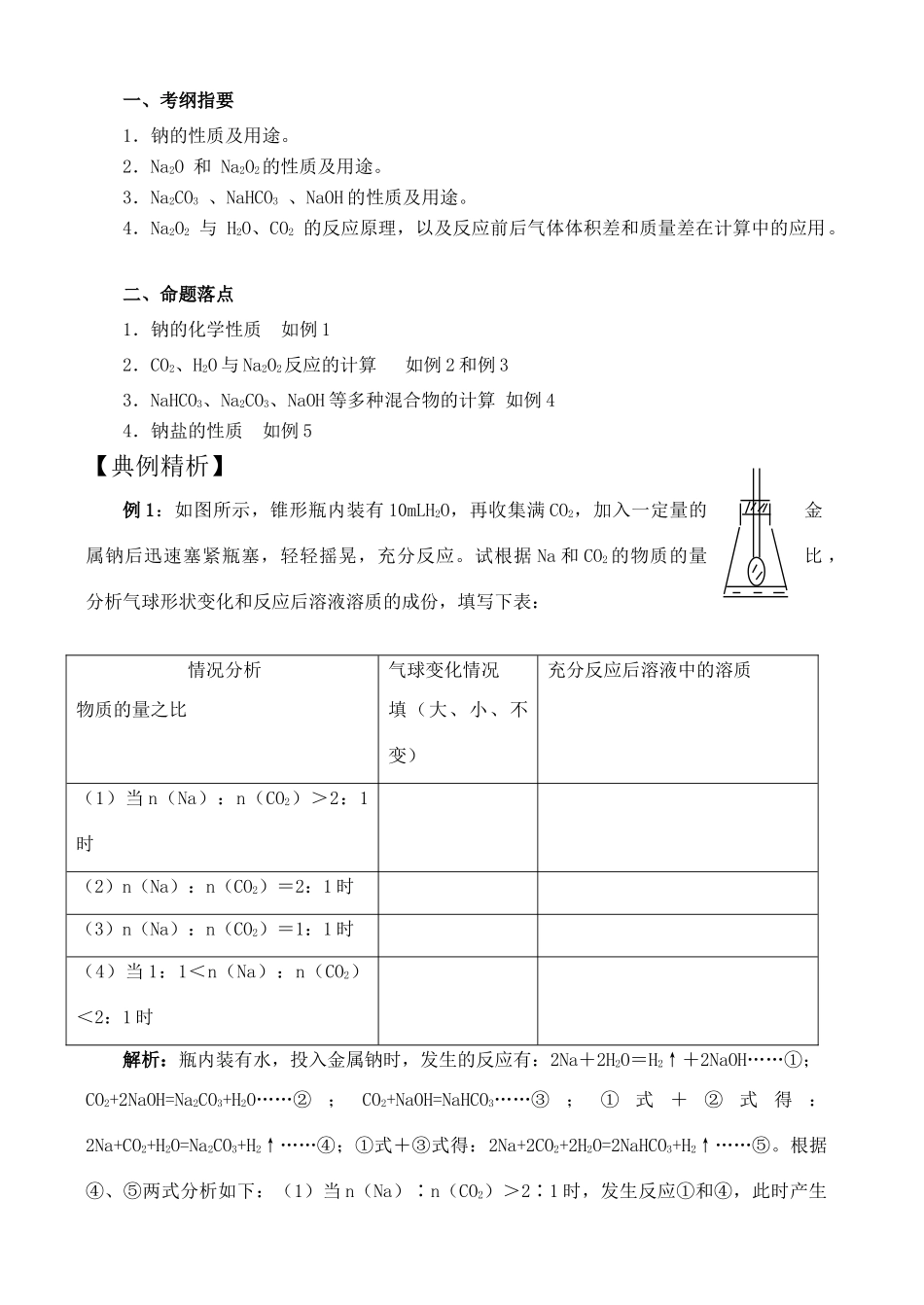
高一化学模块二碱金属【知识网络】一、钠及其化合物之间的关系二、碱金属性质概括第一节钠及其化合物【考点透视】一、考纲指要1.钠的性质及用途
2.Na2O和Na2O2的性质及用途
3.Na2CO3、NaHCO3、NaOH的性质及用途
4.Na2O2与H2O、CO2的反应原理,以及反应前后气体体积差和质量差在计算中的应用
二、命题落点1.钠的化学性质如例12.CO2、H2O与Na2O2反应的计算如例2和例33.NaHCO3、Na2CO3、NaOH等多种混合物的计算如例44.钠盐的性质如例5【典例精析】例1:如图所示,锥形瓶内装有10mLH2O,再收集满CO2,加入一定量的金属钠后迅速塞紧瓶塞,轻轻摇晃,充分反应
试根据Na和CO2的物质的量比,分析气球形状变化和反应后溶液溶质的成份,填写下表:情况分析物质的量之比气球变化情况填(大、小、不变)充分反应后溶液中的溶质(1)当n(Na):n(CO2)>2:1时(2)n(Na):n(CO2)=2:1时(3)n(Na):n(CO2)=1:1时(4)当1:1<n(Na):n(CO2)<2:1时解析:瓶内装有水,投入金属钠时,发生的反应有:2Na+2H2O=H2↑+2NaOH……①;CO2+2NaOH=Na2CO3+H2O……②;CO2+NaOH=NaHCO3……③;①式+②式得:2Na+CO2+H2O=Na2CO3+H2↑……④;①式+③式得:2Na+2CO2+2H2O=2NaHCO3+H2↑……⑤
根据④、⑤两式分析如下:(1)当n(Na)∶n(CO2)>2∶1时,发生反应①和④,此时产生氢气的物质的量大于吸收的CO2的物质的量,所以瓶内压强增大,故气球会被压缩,溶液中的溶质为Na2CO3、NaOH;(2)n(Na)∶n(CO2)=2∶1时,此时只发生反应④,产生的氢气和消耗的CO2的物质的量相等,所以气球形状不变,对应的溶液中的溶质为N