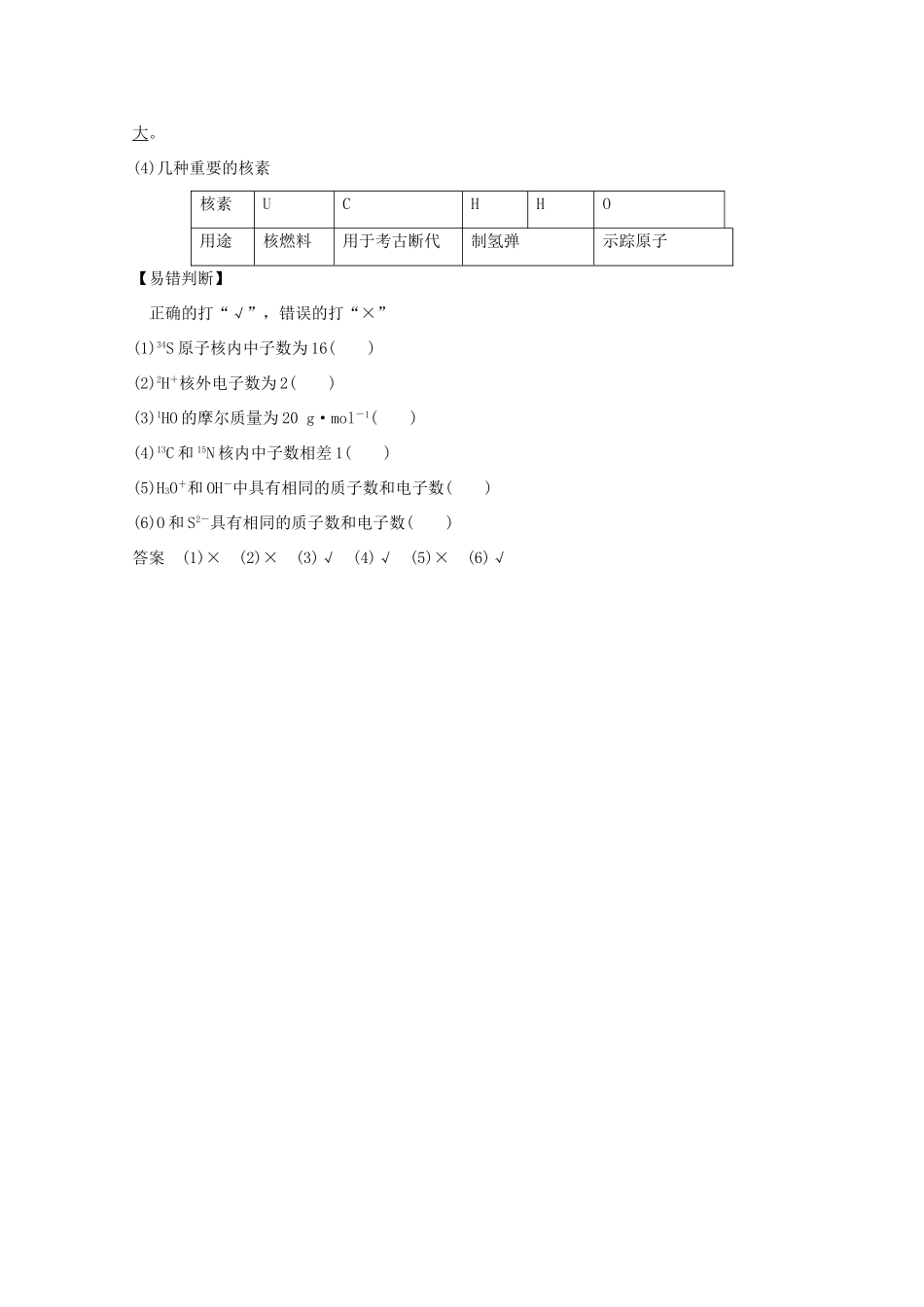
第1单元原子结构与核外电子排布考点一原子的构成[考试标准]1.原子结构模型的演变(a/a)。2.原子的构成,原子符号(b/b)。3.核素、同位素的概念(a/b)。1.原子结构模型的演变—|—|—原子是由原子核和核外电子构成,其中,原子核带正电荷,电子带负电荷。|—2.原子的构成原子3.“三素”——元素、核素、同位素(1)元素符号周围数字的意义(2)元素、核素、同位素的概念及相互关系(3)同位素的性质同一元素的各种核素的中子数不同,质子数相同,化学性质几乎完全相同,物理性质差异较大。(4)几种重要的核素核素UCHHO用途核燃料用于考古断代制氢弹示踪原子【易错判断】正确的打“√”,错误的打“×”(1)34S原子核内中子数为16()(2)2H+核外电子数为2()(3)1HO的摩尔质量为20g·mol-1()(4)13C和15N核内中子数相差1()(5)H3O+和OH-中具有相同的质子数和电子数()(6)O和S2-具有相同的质子数和电子数()答案(1)×(2)×(3)√(4)√(5)×(6)√[归纳总结]原子结构中的微粒关系(1)原子(2)离子的核外电子数核外电子数[考法题组][易错辨析题]1.中新网2013年5月3日报道,Fe的现身揭秘了超新星爆炸历史真相。下列说法中正确的是()A.铁原子的质量数均为60B.Fe的核内质子数比中子数多8C.1molFe与1molFe与足量盐酸反应时均可得到1molH2D.等物质的量的Fe与Fe,前者质量比后者多2g解析60只是“Fe”这种铁原子的质量数,而铁有多种原子,A错误;Fe的核内质子数(26)比中子数(34)少8,B错误;Fe、Fe与盐酸反应时均被氧化成Fe2+,C正确;只有当Fe与Fe均为1mol时,前者质量才比后者多2g,D错误。答案C2.(义乌模拟)重水(D2O)是重要的核工业原料,下列说法错误的是()A.氘(D)原子核外有1个电子B.1H与D互称同位素C.H2O与D2O互称同素异形体D.1HO与DO的相对分子质量相同解析A项,氘表示为H,核外有1个电子;C项,H2O、D2O均为化合物,同素异形体是指同种元素的不同单质;D项,1HO的相对分子质量为20,DO的相对分子质量也为20。答案C[数量关系题]3.用X表示原子:(1)中性原子的中子数N=__________。(2)AXn+共有x个电子,则该阳离子的中子数N=______。(3)AXn-共有x个电子,则该阴离子的中子数N=______。(4)12C16O2分子中的中子数N=________。(5)A2-原子核内有x个中子,其质量数为m,则ngA2-所含电子的物质的量为________。解析根据“质子数+中子数=质量数”的关系,(1)N=A-Z;(2)AXn+共有x个电子,中性原子X的电子数为x+n,则N=A-x-n;(3)AXn-共有x个电子,中性原子X的电子数为x-n,则N=A-x+n;(4)12C16O2分子中的中子数为6+8+8=22;(5)A2-所含电子数为m-x+2,则ngA2-所含电子的物质的量为mol。答案(1)A-Z(2)A-x-n(3)A-x+n(4)22(5)mol考点二原子核外电子排布的规律[考试标准]原子核外电子排布的基本规律(1~18号元素原子结构)(b/c)。1.核外电子排布规律2.原子结构示意图3.核外电子排布与元素性质的关系(1)金属元素原子的最外层电子数一般小于4,较易失去电子,形成阳离子,表现出还原性,在化合物中显正化合价。(2)非金属元素原子的最外层电子数一般大于或等于4,较易获得电子,活泼非金属原子易形成阴离子。在化合物中主要显负化合价。(3)稀有气体元素的原子最外层为8电子(氦为2电子)稳定结构,不易失去或得到电子,通常表现为0价。【应用思考】下图为几种粒子的结构示意图,完成以下填空。(1)属于阳离子结构的粒子是________(填编号,下同)。(2)具有稳定性结构的原子是__________________。(3)只能得电子的粒子是______________;只能失电子的粒子是______________;既能得电子,又能失电子的粒子是_____________________。(4)③粒子半径________④粒子半径(填“大于”、“小于”或“等于”)。(5)某元素R形成的氧化物为R2O3,则R的离子结构示意图可能是________。答案(1)③⑤⑧(2)②(3)③⑤①④⑥⑦⑧(4)小于(5)⑤[归纳总结]常见的等电子微粒(1)“10电子”微粒(2)“18电子”微粒CH3—CH3、H2N—NH2、HO—OH、F—F、F—CH3、CH3—OH……(3)其他等电子微粒①“14电子”微粒:Si、N2、CO、C2H2、C②“16电子”微粒:S、O2、C2H4、HCHO[考法题组][规律应用题]1.下列叙述...