专题十弱电解质的电离平衡和溶液的酸碱性Ⅳ1、氨气溶于水达平衡后,若只改变某一条件,下列说法正确的是()A.继续通入氨气,c(NH4+)·c(OH-)/c(NH3·H2O)会减小B.NH4Cl水解显酸性,所以向溶液中加入NH4Cl固体,会促进NH3·H2O电离C.向溶液加入HCl气体,则一定有c(NH4+)=c(Cl-)D.实验室中可以通过将浓氨水加入到碱石灰中来制取氨气2、室温下,对于0
10mol·L—1的氨水,下列判断正确的是()A.与AlCl3溶液发生反应的离子方程式为Al3++3OH-=Al(OH)3↓B.加水稀释后,溶液中c(NH4+)·c(OH)变大C.用HNO3溶液完全中和后,溶液不显中性D.其溶液的pH=133、25℃,加水稀释10mLpH=11的氨水,下列判断正确的是()A.原氨水的浓度=10-3mol/LB.氨水的电离程度增大,溶液中所有离子的浓度均减小C.溶液中c(NH4+)/c(NH3·H2O)的增大D.再加入10mLpH=3的盐酸,混合液pH=74、室温下,10mL0
1mol·L-1的氨水加水稀释后,下列说法正确的是()A.溶液的pH增大B.溶液中NH4+和OH-离子的数目减少C.NH3·H2O的电离程度增大,c(H+)也增大D.再加入适量盐酸使c(NH4+)=c(Cl-),混合液的pH<75、室温下,下列说法正确的是()A.将pH=2的盐酸和pH=4的硫酸等体积混合,所得溶液pH=3B.HF比HCN易电离,则NaF溶液的pH比同浓度NaCN溶液的pH大C.向0
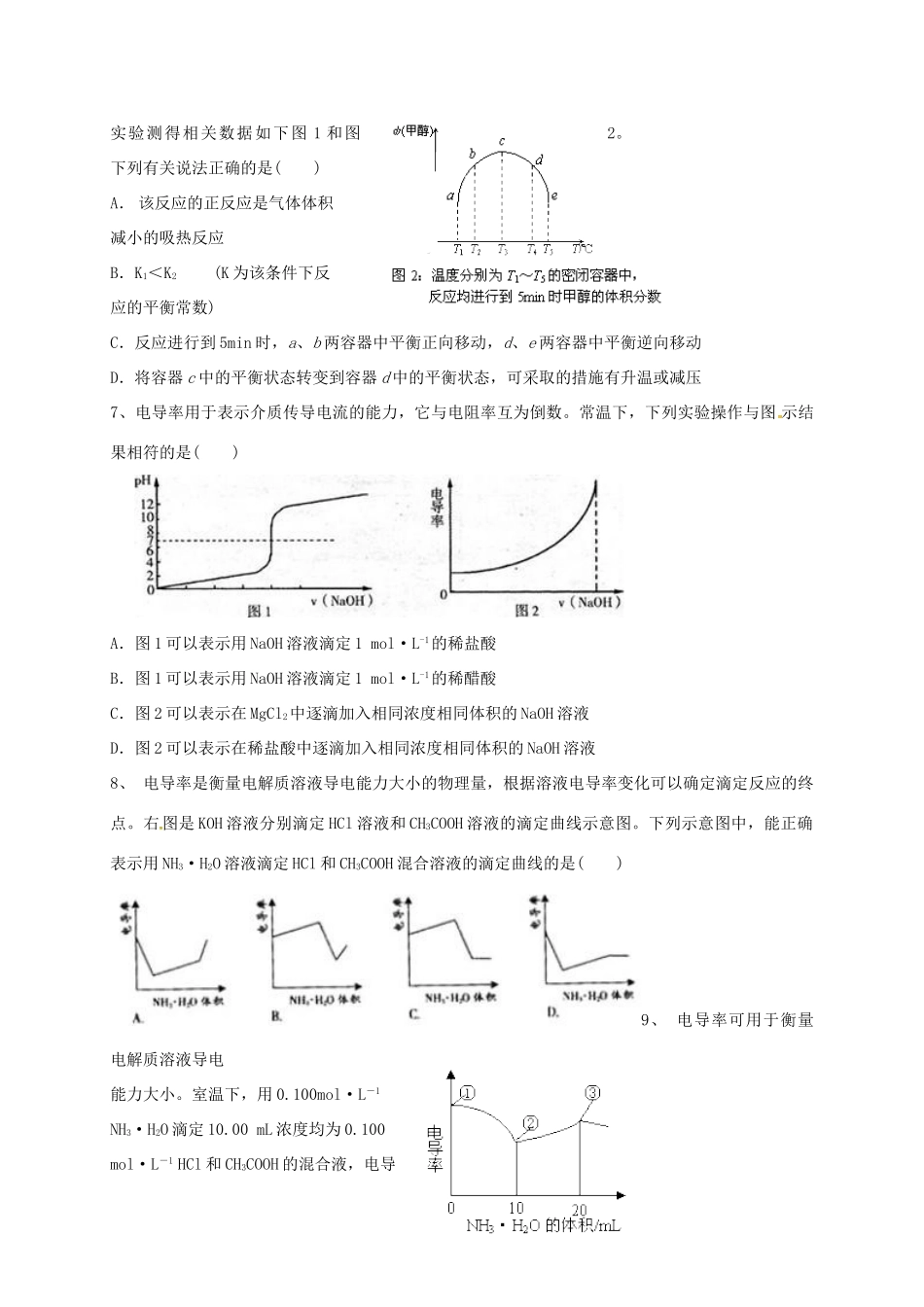
1mol/L氨水中加入少量硫酸铵固体,溶液中c(OH-)/c(NH3·H2O)增大D.将1mLpH=3的HA溶液稀释到10mL,若溶液的pH<4,则HA为弱酸6、CO与H2在催化剂作用下合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g)
在容积均为1L的a、b、c、d、e五个密闭