镜头一:基础实验与基本实验操作可能用到的相对原子质量:H:1C:12N:14O:16Na:23Mg:24Al:27Si:28P:31S:32Cl:35
5Fe:56Cu:64Ag:108Ba:137Cr:521
(5分)(1)玻璃棒是中学化学实验中常用的仪器
下列实验过程中,一般不需要用玻璃棒的是________________(填写编号)①用pH试纸测定Na2CO3溶液的PH②配制一定物质的量浓度的氯化钠溶液③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体④探究Ba(OH)2·8H2O晶体的NH4Cl晶体反应过程中的能量变化⑤实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀(2)用“大于”、“小于”、或“等于”填空:①读取量筒中液体体积时,视线偏高,读取的体积数______________实际体积数
②用托盘天平称取10
4g食盐,将砝码和食盐的位置颠倒,所称取食盐的质量10
③配制500mL0
1mol·L-1NaOH溶液,定容时俯视刻度线,所得溶液的物质的量浓度________________0
1mol·L-1
(16分)实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成
取wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2
现用下图所示装置进行实验(铁架台、铁夹、酒精灯等未画出),请回答有关问题:(1)实验开始时,首先打开止水夹a,通一段时间纯氧,这样做的目的是______;之后则需关闭止水夹a,打开止水夹b
(2)以上装置中需要加热的有(填装置代号)_________
操作时应先点燃_______处的酒精灯
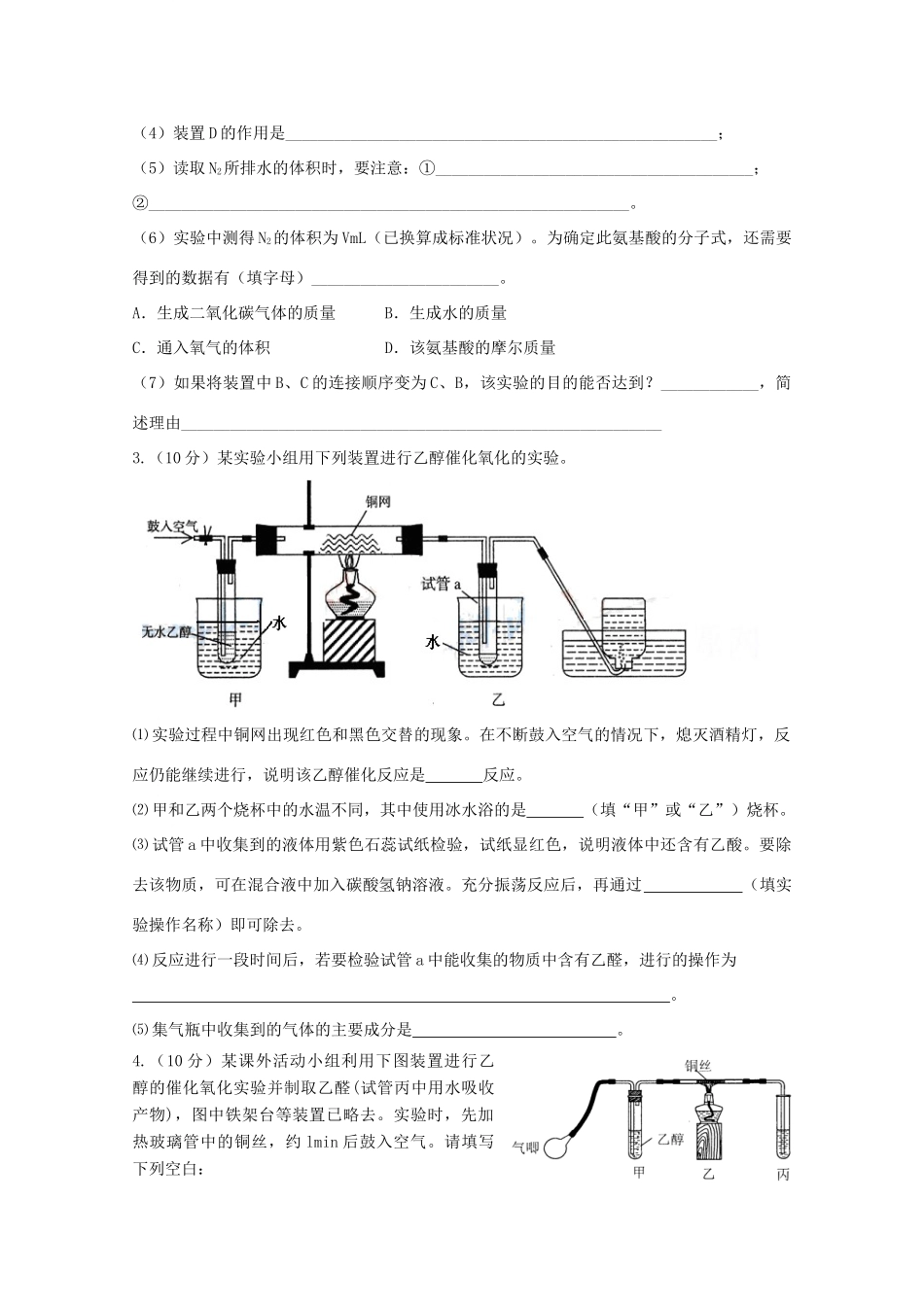
(3)装置A中发生反应的化学方程式为_____________________________________;(4)装置D的作用是___________________________________