专题六氧化还原反应知识点《高考考试说明》对应教材书内容氧化还原在分析元素化合价变化的基础上,理解氧化还原反应的本质(Ⅱ)必修1第二章第三节根据氧化还原反应的规律研究物质的化学性质以及常见氧化剂和还原剂之间的反应(Ⅱ)必修1第二章第三节一、知识整理1.概念凡有电子得失或共用电子对偏移的一类反应称氧化还原反应,其特征是反应前后有元素化合价发生变化
氧化反应和还原反应同时发生,在任何一个氧化还原反应中,得失电子数必定相等
2.物质的氧化性和还原性(1)一般来说,强氧化剂与强还原剂反应后生成的产物,其还原性、氧化性较弱
如强还原性强氧化性弱还原性弱氧化性据此判断:氧化性还原性(2)氧化性、还原性的强弱,取决于物质得失电子的难易,而不取决于得失电子的多少
物质越易得到电子,其氧化性越强,常见的氧化剂有金属阳离子、活泼的非金属单质以及含较高价态元素的物质,如、、、、、浓、等
元素的最高价态物质只具有氧化性,最低价态物质只具有还原性,中间价态物质既具有氧化性,又具有还原性
物质越易失电子,还原性越强,含较低价态元素的物质常作还原剂,常见的还原剂有金属单质、、、、、、等
一般来说,元素的非金属性越强,其单质的氧化性越强;金属的金属性(金属活动性)越弱,则该金属的阳离子的氧化性越强
(3)同种元素间,价态相距越大,发生反应的可能性越大
价态相近或相邻,则难以发生氧化还原反应
如与能反应,与、与(浓)之间不能发生反应
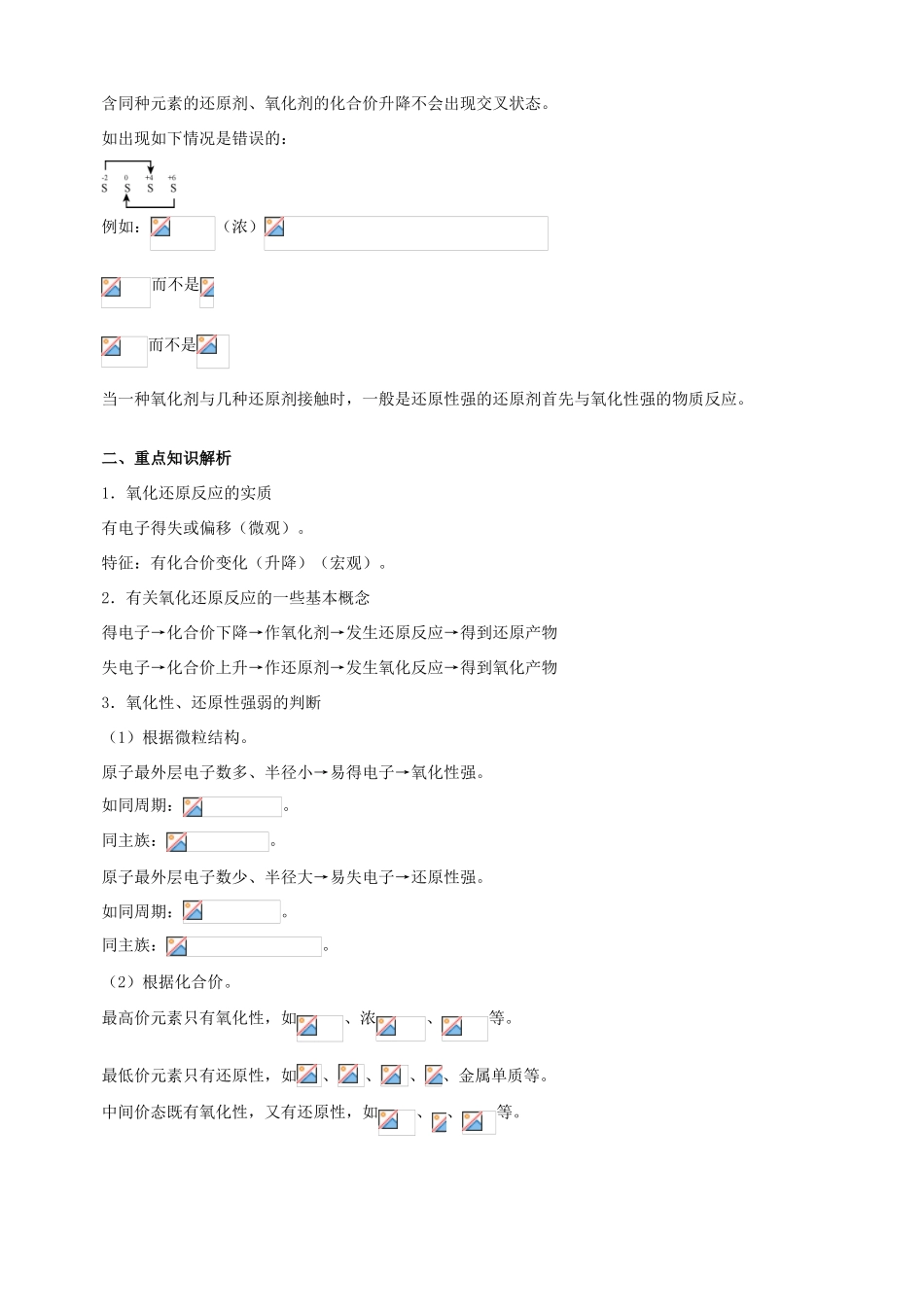
含同种元素的还原剂、氧化剂的化合价升降不会出现交叉状态
如出现如下情况是错误的:例如:(浓)而不是而不是当一种氧化剂与几种还原剂接触时,一般是还原性强的还原剂首先与氧化性强的物质反应
二、重点知识解析1.氧化还原反应的实质有电子得失或偏移(微观)
特征:有化合价变化(升降)(宏观)
2.有关氧化还原反应的一些基本概念得电子→化合价下降→作氧化剂→发生还原反应→得到还原产物失电子→