【优化指导】高考化学总复习课时作业26原电池人教版1.下列有关电池的说法不正确的是()A.原电池负极发生氧化反应B.铅蓄电池工作时,电子沿外电路从铅电极流向二氧化铅电极C.甲醇碱性燃料电池负极附近将有CO2气体放出D.电解质溶液导电过程中必有氧化还原反应发生解析:C项,碱性电池中不会有CO2存在,CO2与OH-会发生反应,故C项错
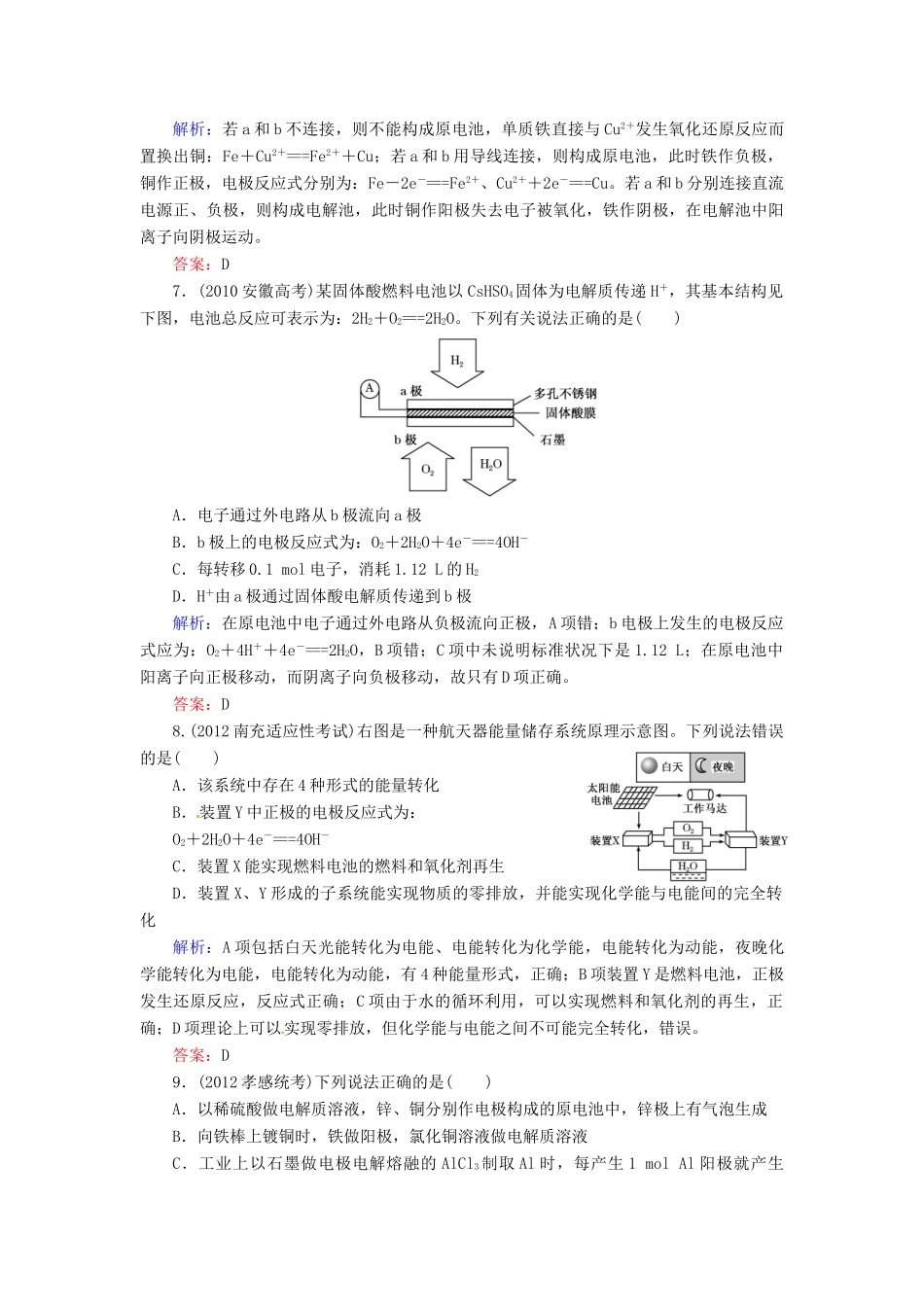
答案:C2.相同材质的铁在图中的四种情况下最不易被腐蚀的是()解析:A、D项,Fe、Cu、醋酸或酸雨形成原电池,Fe为负极,腐蚀较快;B项,发生吸氧腐蚀;C项,铁表面覆盖不活泼的铜镀层,保护了铁,故C项腐蚀最慢
答案:C3.(2010北京高考)下列有关钢铁腐蚀与防护的说法正确的是()A.钢管与电源正极连接,钢管可被保护B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-===Fe3+解析:铁易失去电子,故钢管与电源正极相连时,更易使铁失电子,故A项错;铁遇冷浓硝酸时表面能形成一层致密的氧化膜,故B项正确;铁比铜活泼,当铁、铜相接触时构成原电池,铁作负极被腐蚀,故C项错;钢铁发生析氢腐蚀时,负极发生反应:Fe-2e-===Fe2+,故D项错
答案:B4.(2011北京高考)结合下图判断,下列叙述正确的是()A.Ⅰ和Ⅱ中正极均被保护B.Ⅰ和Ⅱ中负极反应均是Fe-2e-===Fe2+C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-===4OH-D.Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀解析:形成原电池活泼金属作负极,正极均被保护,A项正确;Ⅰ中负极为活泼金属Zn,B项错误;Ⅱ中是酸性溶液,电极反应式中不能有OH-生成,C项错误;Ⅰ中无Fe2+生成,所以无蓝色沉淀生成,D项错误
依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(