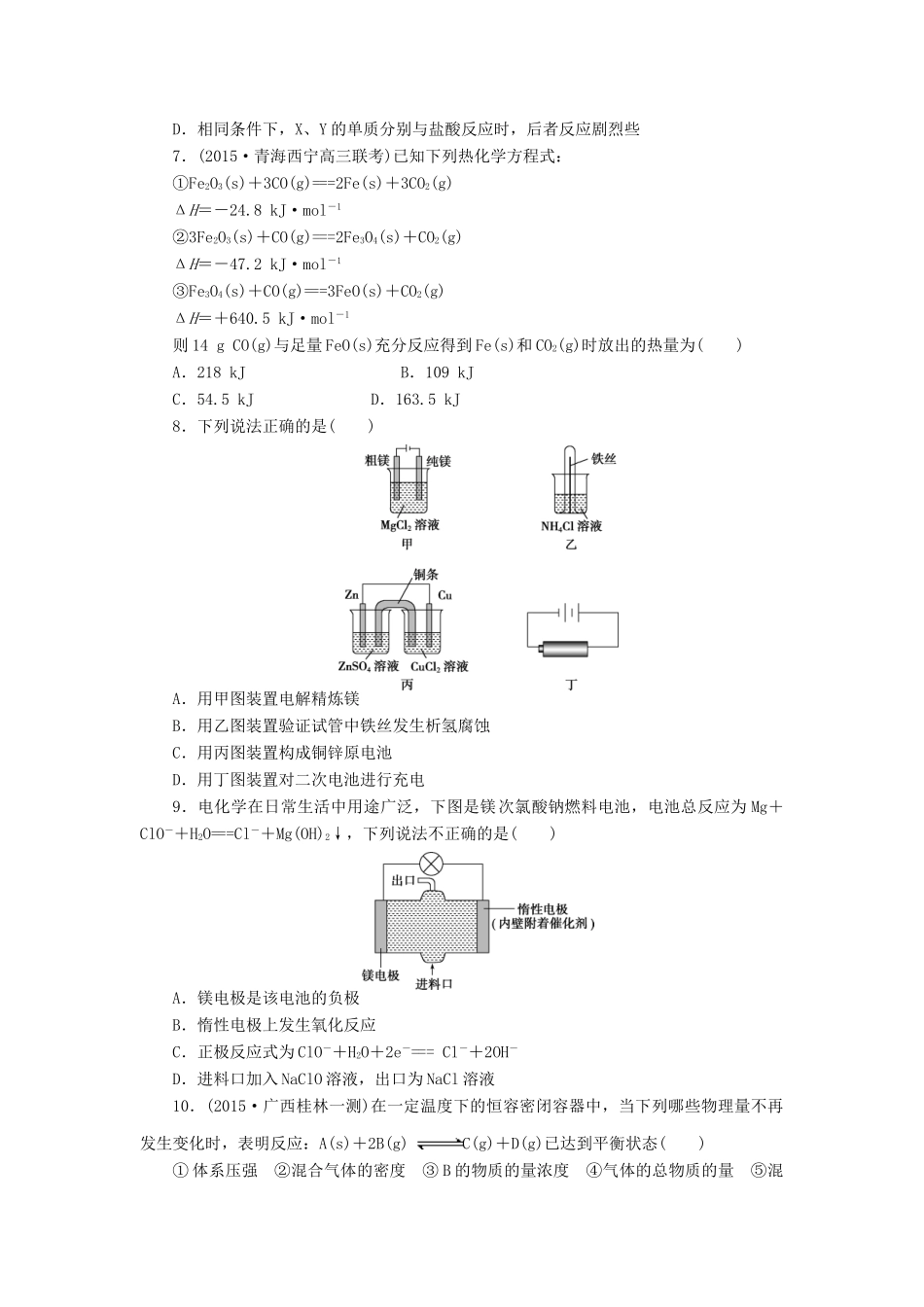
第七题化学基本理论的理解与应用1.(2015·北京朝阳区模拟)合成117号元素的实验中生成了6个新原子,包括5个X和1个X。下列关于X和X的说法不正确的是()A.是两种核素B.互为同位素C.中子数分别为176和177D.电子数相差12.核电荷数为1~18的元素中,下列叙述正确的是()A.最外层只有1个电子的元素一定不是非金属元素B.最外层只有2个电子的元素一定是金属元素C.原子核外各层电子数相等的元素一定是非金属元素D.核电荷数为17的元素的原子容易获得1个电子3.(2015·广东江门期末)下列有关叙述正确的是()A.O和O中子数相同,质子数不同,互为同位素B.H2O比H2S稳定,H—S键比H—O键更难断裂C.Na2O晶体中存在离子键,是离子化合物D.Na2O2晶体中阳离子与阴离子个数比为1∶14.(2015·山东烟台模拟)X、Y、Z三种短周期元素在周期表中的相对位置如图所示,Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是()A.在三种元素形成的气态氢化物中,Y的气态氢化物最稳定B.Z元素的氧化物对应的水化物一定是一种强酸C.三种元素原子半径的大小顺序为X>Y>ZD.Z的单质与Fe反应生成的化合物中,铁元素显+3价5.(2015·北京海淀区模拟)现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法正确的是()A.简单阳离子的氧化性:Y>XB.气态氢化物的稳定性:Z>MC.简单离子半径由大到小的顺序:Z>M>YD.等物质的量浓度的X2Z与Y2Z的溶液中,水的电离程度:X2Z>Y2Z6.几种短周期元素的原子半径及主要化合价如表所示:元素代号XYZW原子半径/pm1601437066主要化合价+2+3+5、+3、-3-2下列叙述正确的是()A.Z的最高价氧化物对应水化物与其氢化物能发生化合反应生成离子化合物B.一定条件下,Z的单质与W的常见单质直接生成ZW2C.Y的最高价氧化物对应水化物能溶于氨水D.相同条件下,X、Y的单质分别与盐酸反应时,后者反应剧烈些7.(2015·青海西宁高三联考)已知下列热化学方程式:①Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)ΔH=-24.8kJ·mol-1②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g)ΔH=-47.2kJ·mol-1③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g)ΔH=+640.5kJ·mol-1则14gCO(g)与足量FeO(s)充分反应得到Fe(s)和CO2(g)时放出的热量为()A.218kJB.109kJC.54.5kJD.163.5kJ8.下列说法正确的是()A.用甲图装置电解精炼镁B.用乙图装置验证试管中铁丝发生析氢腐蚀C.用丙图装置构成铜锌原电池D.用丁图装置对二次电池进行充电9.电化学在日常生活中用途广泛,下图是镁次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O===Cl-+Mg(OH)2↓,下列说法不正确的是()A.镁电极是该电池的负极B.惰性电极上发生氧化反应C.正极反应式为ClO-+H2O+2e-===Cl-+2OH-D.进料口加入NaClO溶液,出口为NaCl溶液10.(2015·广西桂林一测)在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明反应:A(s)+2B(g)C(g)+D(g)已达到平衡状态()①体系压强②混合气体的密度③B的物质的量浓度④气体的总物质的量⑤混合气体的总质量A.②③⑤B.①②③C.②③④D.①③④⑤11.(2015·黑龙江哈尔滨模拟)对于反应4A+2B3C,下列说法中正确的是()A.某温度时,化学反应速率无论用A、B、C中任何物质表示,其数值都相同B.其他条件不变时,降低温度,化学反应速率减小C.其他条件不变时,增大压强,化学反应速率一定加快D.若增大或减小A的物质的量,化学反应速率一定会发生明显的变化12.(2015·海南海口二检)下列说法正确的是()A.工业生产硫酸中采用高温可提高二氧化硫的转化率B.合成氨工业中,适当高的温度既可以提高反应速率,又可以使催化剂的活性最大C.用氢氧化钠溶液吸收二氧化碳气体,升高温度可使吸收速率加快D.酯化反应是一个可逆的吸热反应,故温度越高越有利于生成酯13.(2015·贵州十二校联考)在一固定容积的密闭容器中,加入2molI2和1molH2,发生反应:H2(g)+I2(g)2HI(g),达到平衡时HI的体积分数为b%。若维持容器容积和温度不变,下列四种配比作为起始物质,达新平衡时HI的体积分数为b%的是()A.4molI2+...