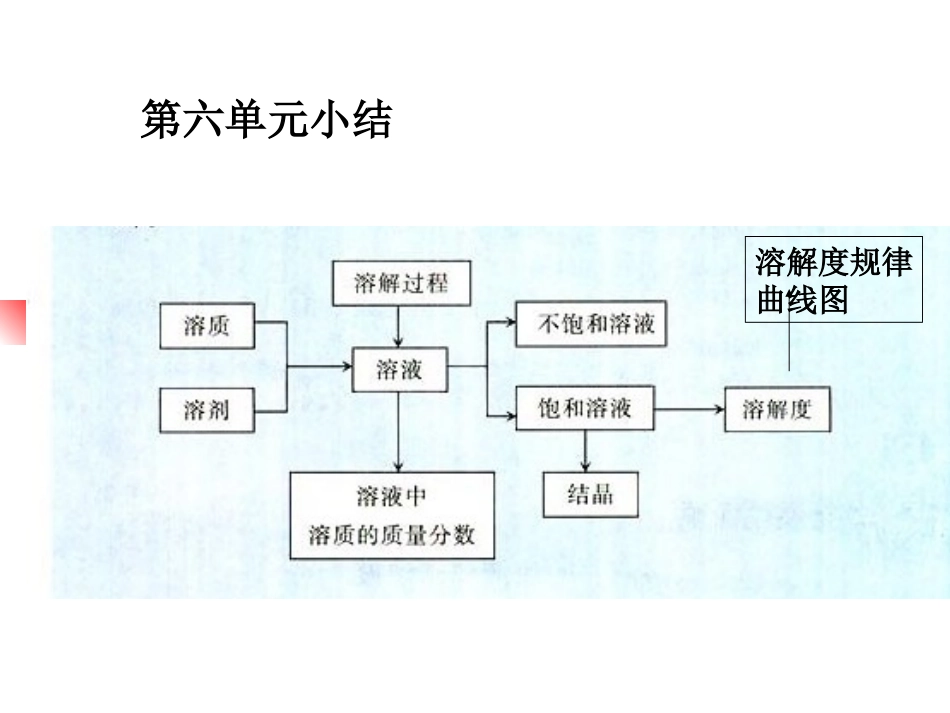
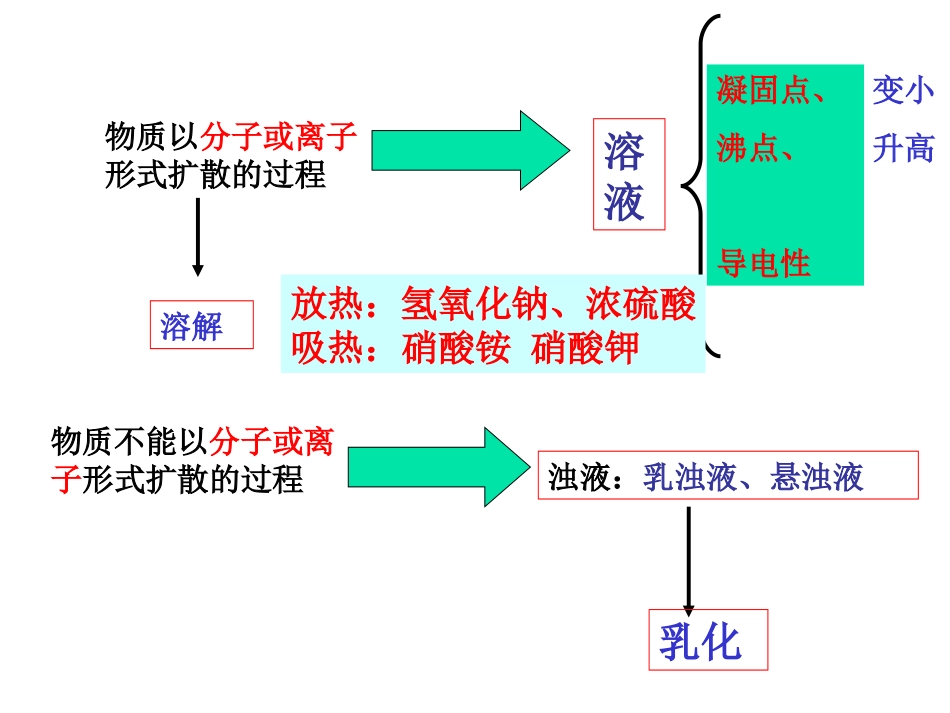
第六单元小结溶解度规律曲线图物质以分子或离子形式扩散的过程溶液浊液:乳浊液、悬浊液凝固点、沸点、导电性放热:氢氧化钠、浓硫酸吸热:硝酸铵硝酸钾物质不能以分子或离子形式扩散的过程溶解乳化变小升高1
溶液定义:定义:一种或几种物质分散到另一种物质里,一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物就是溶液
形成均一的、稳定的混合物就是溶液
溶质溶质溶剂溶剂均一均一····稳定稳定····混合物混合物⑶⑶溶液是由溶液是由溶质溶质和和溶剂溶剂所组成
能溶解其他物质的能溶解其他物质的物质叫做溶剂
物质叫做溶剂
被溶解的被溶解的物质叫做溶物质叫做溶质;质;⑴⑴溶液的特征是:溶液的特征是:均一性、稳定性均一性、稳定性
⑵溶液是混合物混合物
溶液组成的判断1、典型溶液:稀盐酸、石灰水、碘酒、稀硫酸、植物油的汽油溶液2、放入水中变化的物质:氧化钙溶质:
Ca(OH)2CuSO4
5H2OCuSO42
溶液的性质—沸点凝固点导电性的条件:电子离子导电的物质:金属和石墨(自由移动的电子)部分溶液(自由移动的离子)1、判断下列物质是否导电
NaOH固体食盐固体HCl的水溶液KNO3固体KNO3溶液蔗糖溶液酒精溶液要求有自由移动的带电微粒氯化钠溶于水微观示意图微粒种类:水分子钠离子氯离子定义饱和溶液:在一定温度下,在一定量的溶剂里不能再溶解某种溶质的溶液叫做这种溶质的饱和溶液
不饱和溶液:还能再继续溶解某种溶质的溶液3
饱和溶液与不饱和溶液判断方法:1
有无晶体析出2
再加溶质能否继续溶解饱和溶液与不饱和溶液的转化:降低温度饱和溶液增加溶剂升高温度蒸发溶剂增加溶质不饱和溶液需要注意:溶液是否饱和与浓稀没有直接关系
浓溶液可以是不饱和溶液,比如酒精溶液2
稀溶液可以是饱和溶液,比如氢氧化钙溶液3
饱和溶液一定是该温度下的浓溶液定义:4
影响物质溶解性的因素(1)不同物质在同