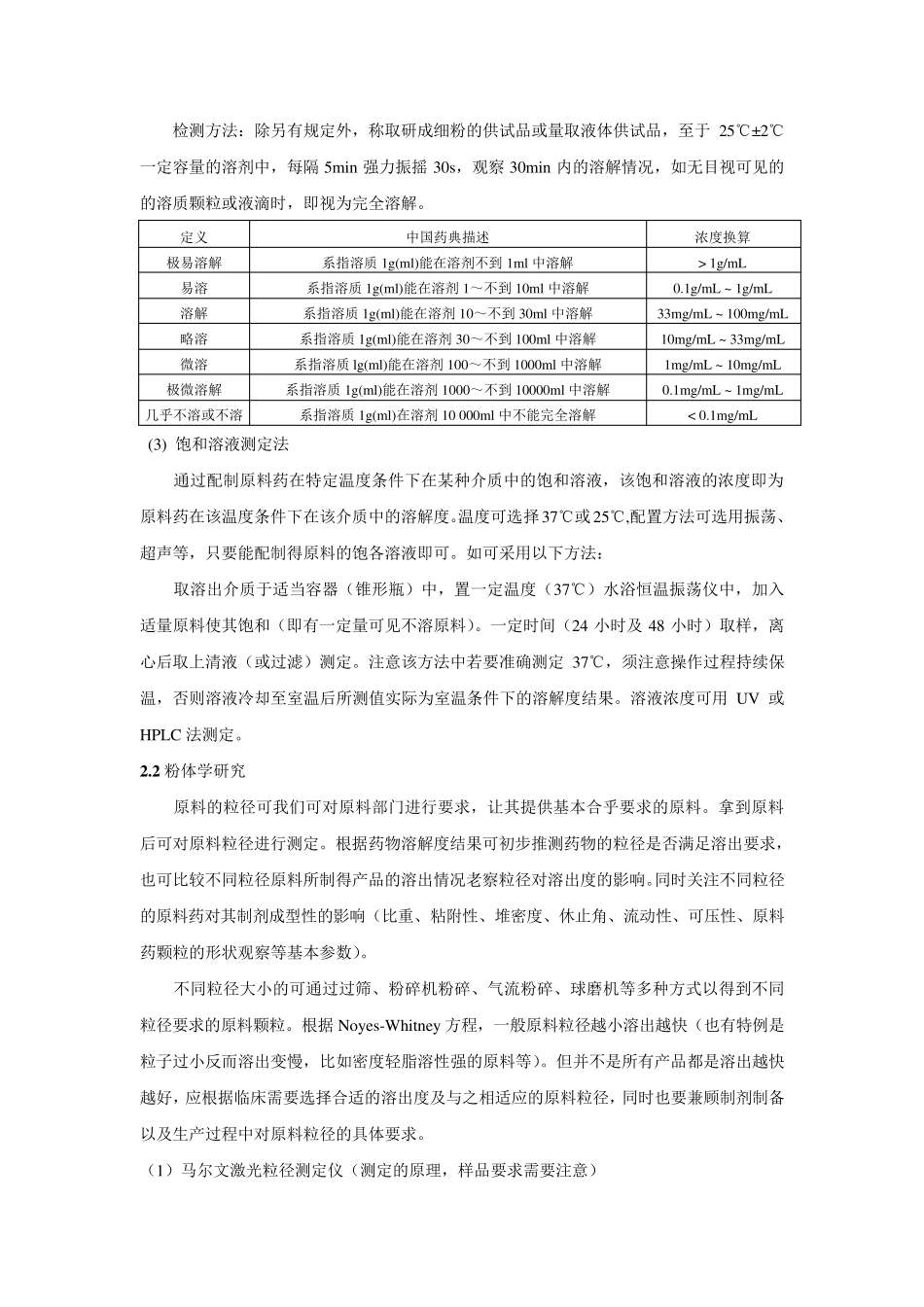
制剂研发的基本工作基本流程(主要环节) 基本流程 1 相关文献资料调研等前期准备 2 处方前研究(基本理化性质等) 3 原辅料相容性研究 4 处方工艺筛选和优化 5 影响因素实验 6 小试稳定性样品制备和稳定性研究 7 中试放大和中试稳定性研究 1 相关文献资料调研等前期准备 主要对其原料药进行资料调研。主要包括与制备制剂以及体内过程可能相关的各种基本理化性质,比如lo gP 值(脂溶性如何以及可能的溶剂)、p Ka 值(酸碱性,尤其对注射剂)、溶解度(不同 p H 值和性质的溶出/溶解体系,初步判断是否具有 p H 值依赖等)、渗透性(初步判断其在体内的吸收与否)、晶型(晶型的不同,药物溶解性及稳定性有可能不同)、药物的剂型及规格、作用机制(靶点以及发挥作用的路径等)、药理毒理信息(有效治疗浓度和中毒剂量判断)、药动学行为(整个的ADME 过程及各自的特点),相关制剂的上市信息、临床信息、专利情况以及有关的文献资料(综述或者具体研究)等。 对其以上市产品进行信息调研。包括其上市产品说明书,涉及大量的不良反应、临床治疗学、群体药动学等相关资料。还有国内及进口制剂剂型、规格以及相关特点(改剂型时尤其注意);产品的质量标准(原研标准、国内首仿标准、药典标准。这些标准能否弄到,并要比较不同标准的异同和实时标准更新);原研处方组成及工艺研究资料(有时需要注意原研处方未必是最优处方);原研处方中辅料情况(是否都可买到及是否有标准,有否进口);药品稳定性资料(关注杂质变化、限度及其原因);国内外专利情况(是否侵权及能否避开);生产注册情况(产品原研厂家、国内生产申报厂家,注册与正式产品之间有差异,需要分析原因);参比制剂的来源(通过对参比制剂的研究,如对外观、性状、溶出情况等等的观察,以及对含量、溶出度、有关物质、硬度、片重(装量)等参数的测定,往往能得到一些对项目开发有重要参考价值的数据或资料)。 最后要对所有信息进行汇总形成该研药物的制剂研发调研报告,内容要包括或参比制剂的相关信息概述、所研药物制剂的开发策略、各阶段的原料大概需求、各阶段的研究时间表、 研究过程可能遇到或者出现的问题以及初步的解决方案等。该立题报告要突出调研二字,不能是信息的大杂烩,而应该是经过自己的信息提炼、分析和总结后得出的切实可行的项目开展方案。 2 处方前研究(基本理化性质等) 进行相关处方前的研究工作:主要包括溶解度研...