第一章气体1 两个容积均为V 的玻璃球泡之间用细管连结,泡内密封着标准状态下的空气
若将其中的一个球加热到 100℃,另一个球则维持0℃,忽略连接细管中气体
解:由题给条件知,(1)系统物质总量恒定;(2)两球中压力维持相同
2 一密闭刚性容器中充满了空气,并有少量的水
但容器于300 K 条件下大平衡时,容器内压力为101
325 kPa
若把该容器移至373
15 K 的沸水中,试求容器中到达新的平衡时应有的压力
设容器中始终有水存在,且可忽略水的任何体积变化
300 K 时水的饱和蒸气压为3
567 kPa
解:将气相看作理想气体,在300 K 时空气的分压为由于体积不变(忽略水的任何体积变化),373
15 K 时空气的分压为由于容器中始终有水存在,在373
15 K 时,水的饱和蒸气压为101
325 kPa,系统中水蒸气的分压为 101
325 kPa,所以系统的总压K15
373,OHPairPP2=(121
595 + 101
325)KPa =222
92KPa 第二章 热力学第一定律1
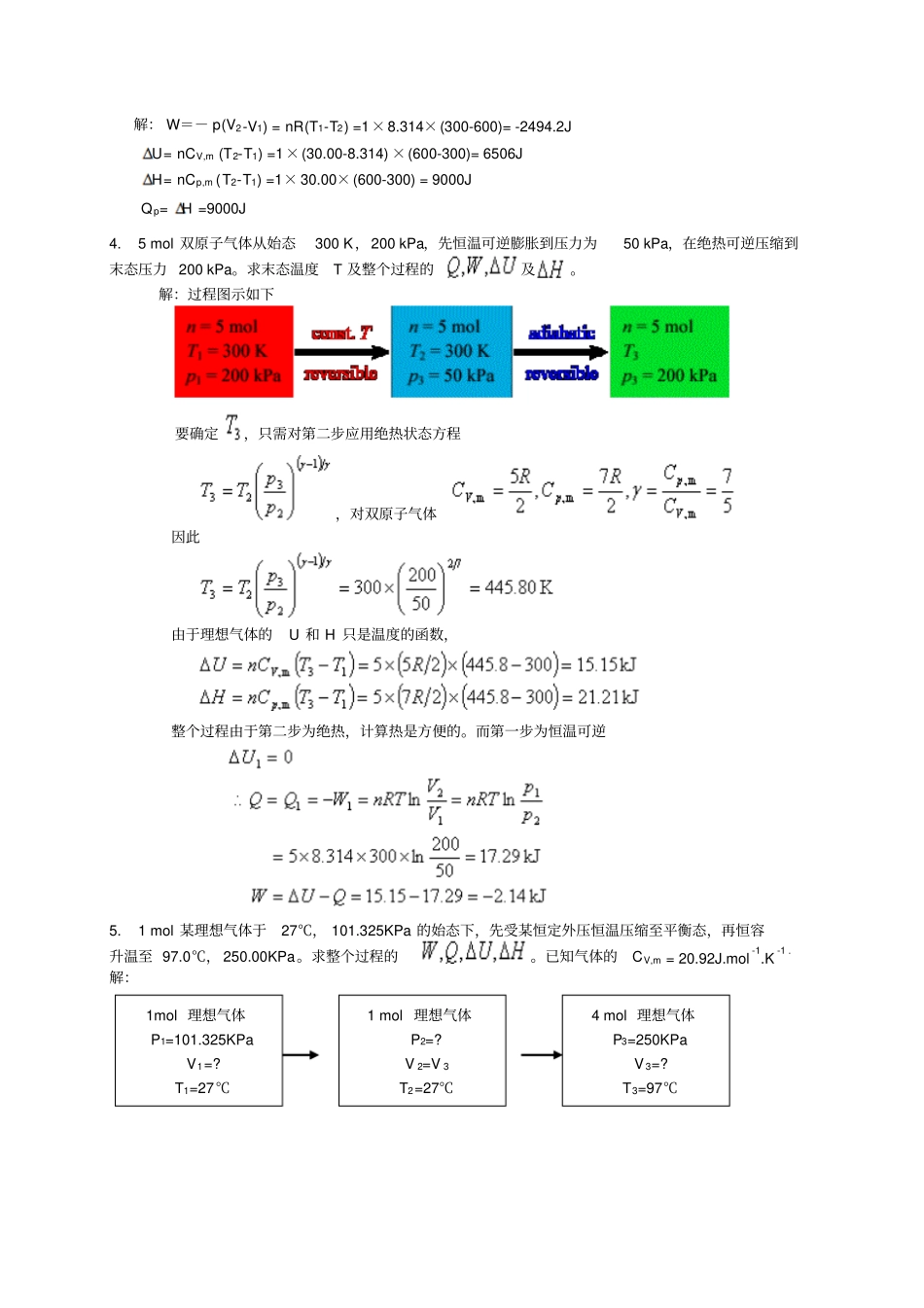
1mol 理想气体经如下变化过程到末态,求整个过程的W、Q、△ U、△ H
解:KnRVPTKnRVPTKnRVPT7
243314
81101105
20262437314
811010105
243314
8110101065
202333333322233111恒容升温过程:W 1= 0 J 恒容1 mol 理想气体P2=2026
5 KPa V 2=10dm3T 2=
1 mol 理想气体P1=202
65 KPa V 1=10 dm3T 1=
1 mol 理想气体P3=2026
5 KPa V 3=1 dm3T3=
恒压恒压压缩过程:W 2= - P 外(V 3- V 1) = - 2026
5×103×(1- 10)×10-3=18