5电解质溶液的活度和活度系数1
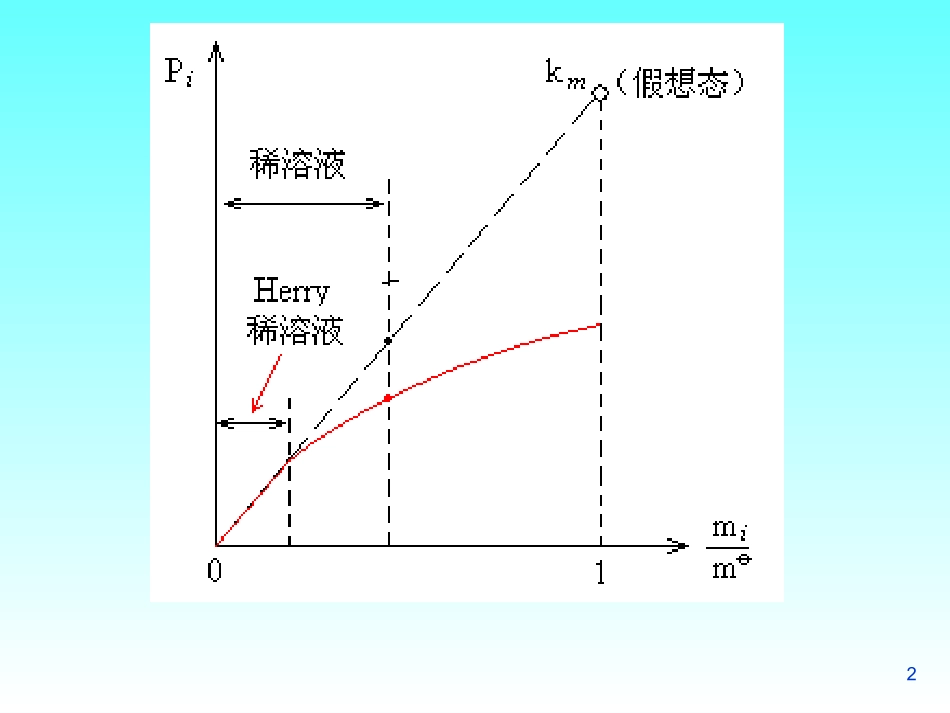
服从Henry定律的稀溶液一、活度a、活度系数的引出i=i(T,km)+RTln(mi/m)式中:m=1mol/kg;i(T,km):标准态化学势,为浓度mi=m,且满足Henry定律:Pig=km(mi/m)=km的假想态化学势
一般稀溶液中,组分i对Henry定律有偏差1)式中i(T)表示假想的标准状态:mi=m,且满足Henry定律(i=1)的状态的化学势;2)活度ai及活度系数i均为无量纲量;3)上述i为非电解质组分i在水溶液中的化学势
i=i(T)+RTlnaiiiimmai=i(T)+RTlnaiiiimma4二、电解质溶液的活度、活度系数1
电解液中组分i的活度ai电解液中组分的构成较非电解质溶液要复杂
通常强电解质溶于水后,完全电离成正、负离子,不考虑生成离子对(IP)
5如:电解质M+Z+AZ溶于水
完全电离后:M+A+MZ++AZ体系自由能变化(完全电离):dG=SdT+VdP+ldnl+idni(溶剂)(溶质)其中电解质溶质引起的化学势变化:6idni=+dn++dn=+(+dni)+(dni)=(+++)dnidG=SdT+VdP+ldnl+idni代入化学势定义式,得电解质i的化学势:ln,P,Tii)nG(7+=+(T)+RTlna+其中:a+=(m+/m)+,a+为离子活度;+为离子活度系数;+(T)为假想标准态(m+=m,且+=1)的化学势
则电解质i(M+A)的“化学势”可化成:离子的化学势表达式,类似于非电解质溶质分子:8i=+++=+[+(T)+RTlna+]