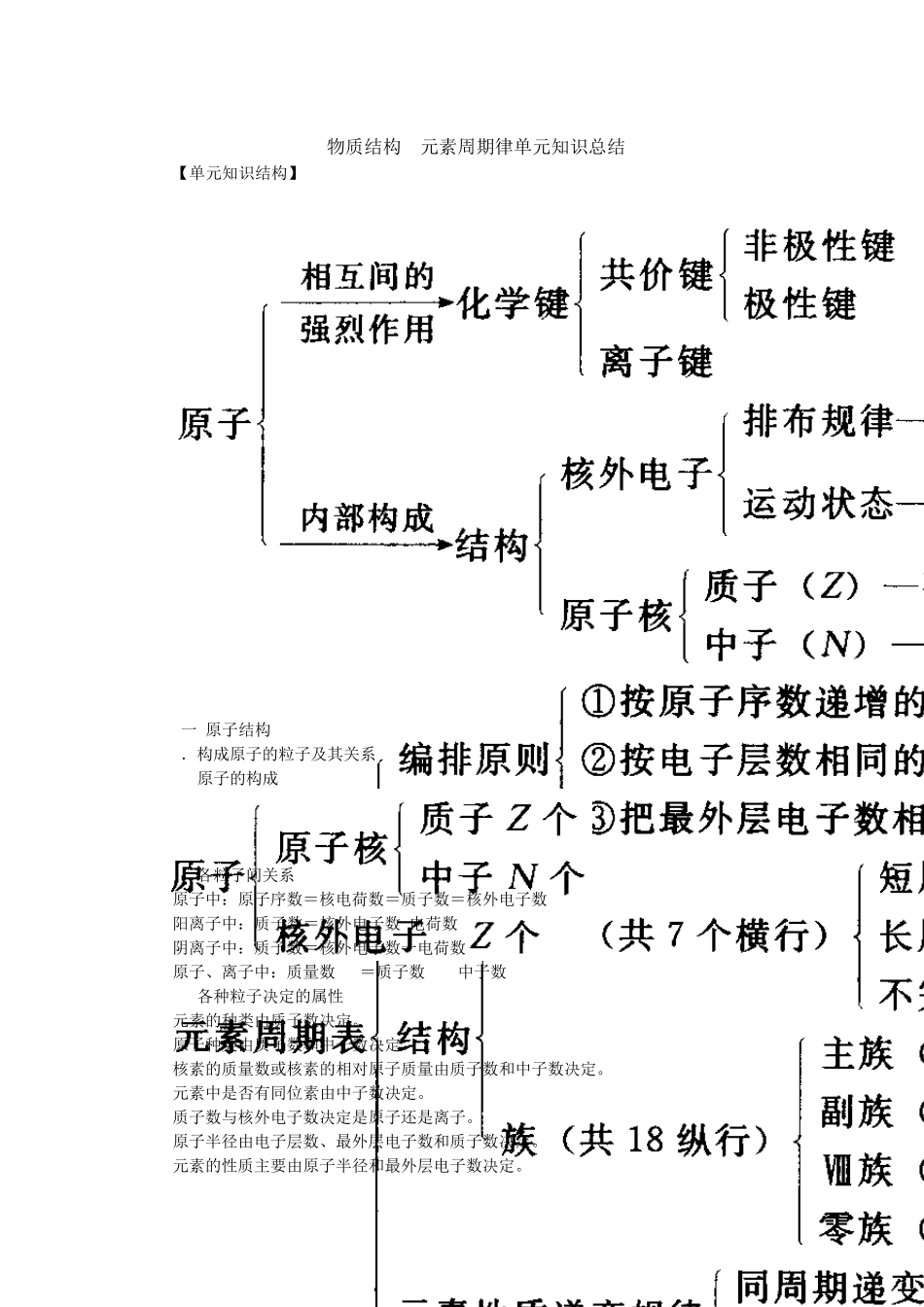
物质结构 元素周期律单元知识总结 【单元知识结构】 (一)原子结构 1.构成原子的粒子及其关系 (1)原子的构成 (2)各粒子间关系 原子中:原子序数=核电荷数=质子数=核外电子数 阳离子中:质子数=核外电子数+电荷数 阴离子中:质子数=核外电子数一电荷数 原子、离子中:质量数(A)=质子数(Z)+中子数(N) (3)各种粒子决定的属性 元素的种类由质子数决定
原子种类由质子数和中子数决定
核素的质量数或核素的相对原子质量由质子数和中子数决定
元素中是否有同位素由中子数决定
质子数与核外电子数决定是原子还是离子
原子半径由电子层数、最外层电子数和质子数决定
元素的性质主要由原子半径和最外层电子数决定
(4)短周期元素中具有特殊性排布的原子 最外层有一个电子的非金属元素:H
最外层电子数等于次外层电子数的元素:Be、Ar
最外层电子数是次外层电子数2、3、4倍的元素:依次是 C、O、Ne
电子总数是最外层电子数2倍的元素:Be
最外层电子数是电子层数2倍的元素:He、C、S
最外层电子数是电子层数3倍的元素:O
次外层电子数是最外层电子数2倍的元素:Li、Si
内层电子总数是最外层电子数2倍的元素:Li、P
电子层数与最外层电子数相等的元素:H、Be、Al
2.原子、离子半径的比较 (1)原子的半径大于相应阳离子的半径
(2)原子的半径小于相应阴离子的半径
(3)同种元素不同价态的离子,价态越高,离子半径越小
(4)电子层数相同的原子,原子序数越大,原子半径越小(稀有气体元素除外)
(5)最外层电子数相同的同族元素的原子,电子层数越多原子半径越大;其同价态的离子半径也如此
(6)电子层结构相同的阴、阳离子,核电荷数越多,离子半径越小
3.核素、同位素 (1)核素:具有一定数目的质子和一定数目的中子的一种原子
(2)同位素:同一元