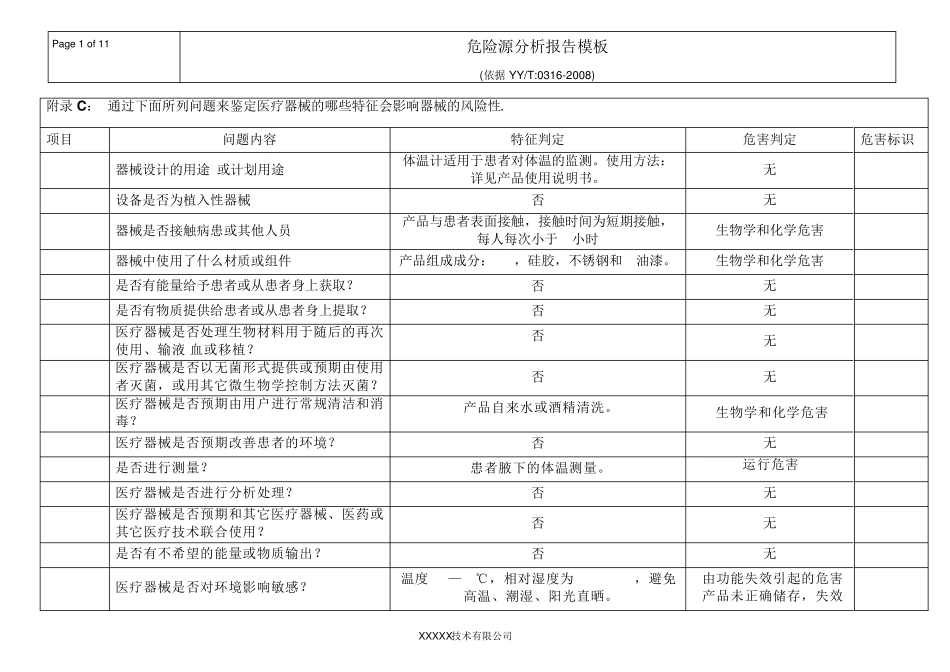
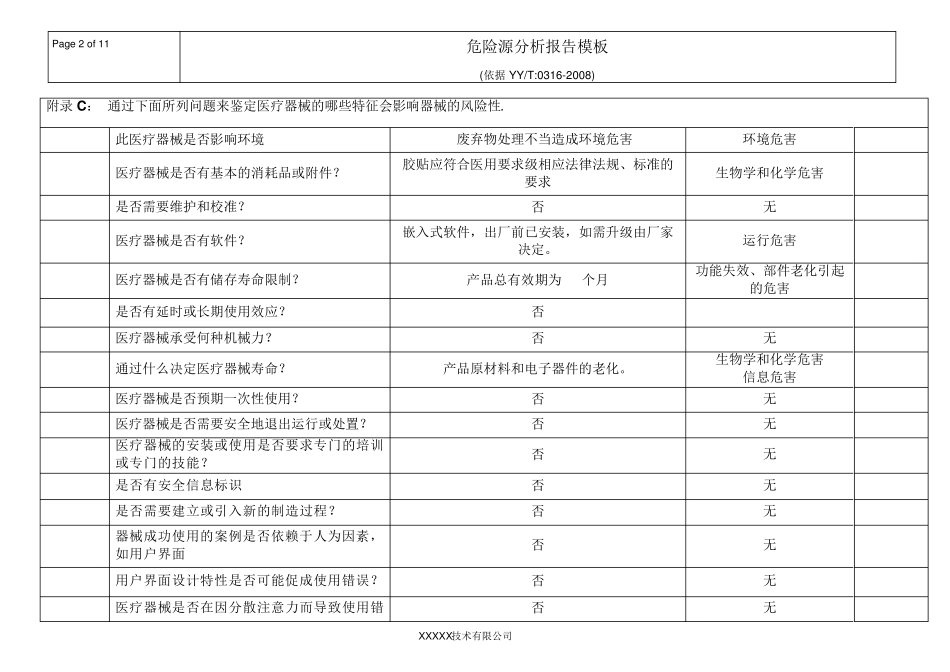
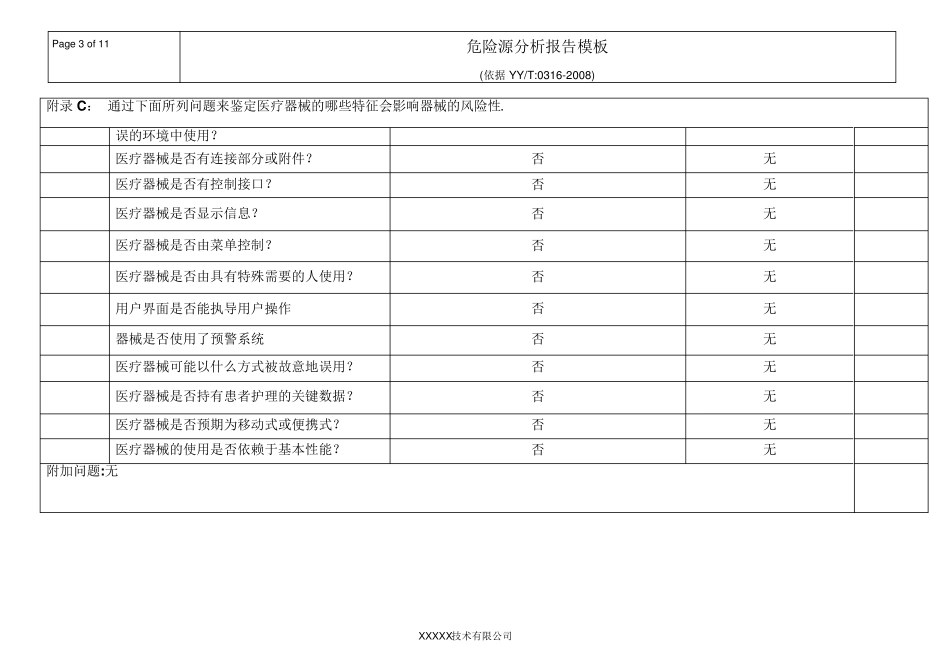
Pag e 1 o f 11 危险源分析报告模板 (依据 YY/T:0316-2008) XXXXX技术有限公司 附录 C : 通过下面所列问题来鉴定医疗器械的哪些特征会影响器械的风险性
项目 问题内容 特征判定 危害判定 危害标识 C
1 器械设计的用途/或计划用途 体温计适用于患者对体温的监测
使用方法:详见产品使用说明书
2 设备是否为植入性器械 否 无 C
3 器械是否接触病患或其他人员 产品与患者表面接触,接触时间为短期接触,每人每次小于24小时 生物学和化学危害 H1 C
4 器械中使用了什么材质或组件 产品组成成分:ABS,硅胶,不锈钢和UV油漆
生物学和化学危害 H2 C
5 是否有能量给予患者或从患者身上获取
6 是否有物质提供给患者或从患者身上提取
7 医疗器械是否处理生物材料用于随后的再次使用、输液/血或移植
8 医疗器械是否以无菌形式提供或预期由使用者灭菌,或用其它微生物学控制方法灭菌
9 医疗器械是否预期由用户进行常规清洁和消毒
产品自来水或酒精清洗
生物学和化学危害 H3 C
10 医疗器械是否预期改善患者的环境
11 是否进行测量
患者腋下的体温测量
运行危害 H4 C
12 医疗器械是否进行分析处理
13 医疗器械是否预期和其它医疗器械、医药或其它医疗技术联合使用
14 是否有不希望的能量或物质输出
15 医疗器械是否对环境影响敏感
温度-20—55℃,相对湿度为15% - 85%,避免高温、潮湿、阳光直晒
由功能失效引起的危害 产品未正确储存,失效 H5 Pag e 2 o f 11 危险源分析报告模板 (依据 YY/T:0316-2008) X