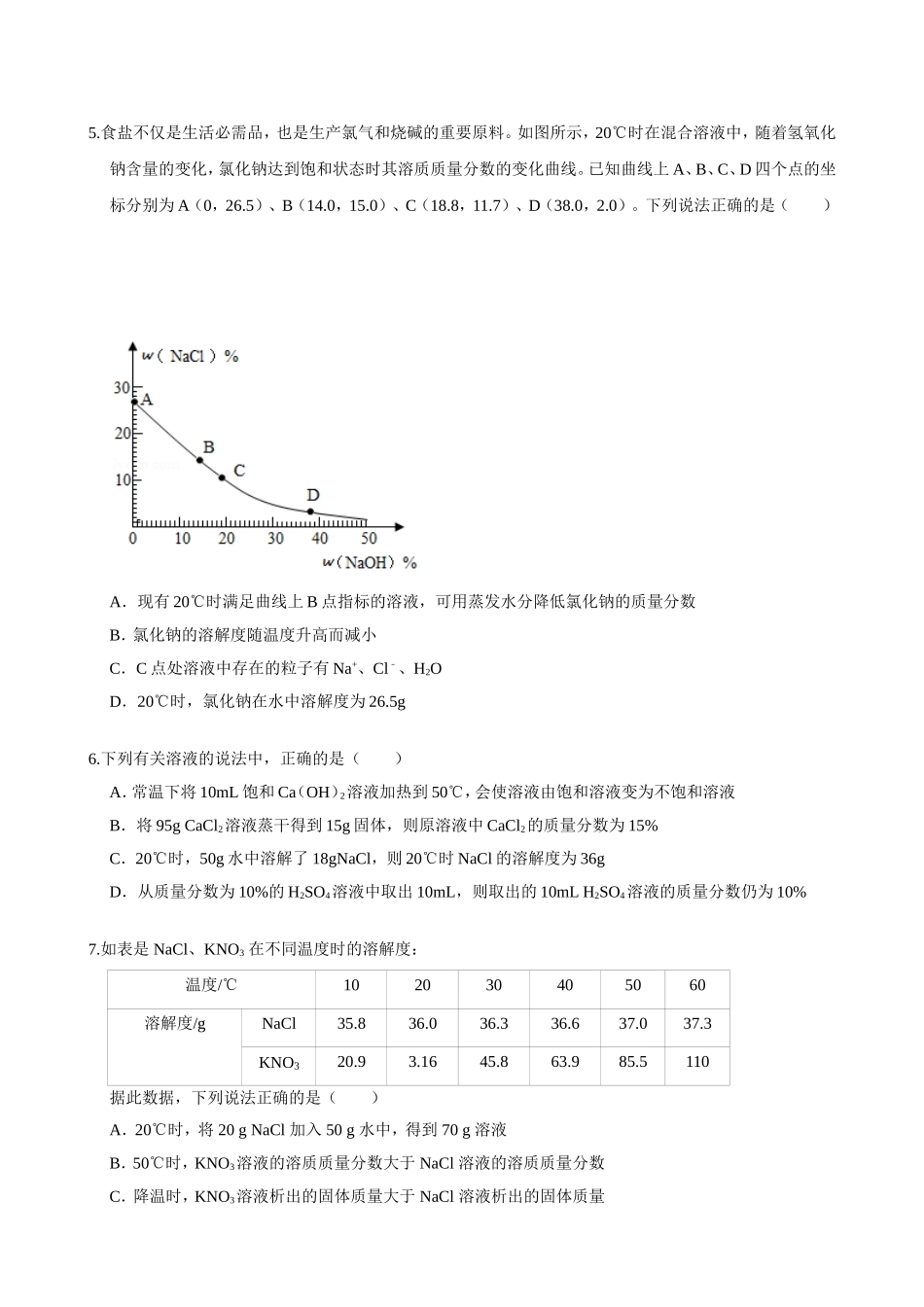
质量分数C学校:________班级:________姓名:________学号:________一、单选题(共15小题)1.某温度时,将烧杯中的xgKNO3饱和溶液恒温下蒸发部分溶剂,然后再将烧杯中的物质逐渐升温(假设升温时溶剂没有损失),能够正确表示此过程中KNO3溶液溶质的质量分数(w)与时间(t)关系的示意图是()A.B.C.D.2.表是氯化钠硝酸钾在不同温度时的溶解度:(溶解度/g)温度/℃2030405060氯化钠36.036.336.637.037.3硝酸钾31.645.863.985.5110据此数据,判断下列说法错误的是()A.在20℃~30℃温度范围内,硝酸钾和氯化钠的溶解度会相等B.在60℃时,硝酸钾的饱和溶液105g加入95g水后溶液中溶质的质量分数为27.5%C.在20℃时,氯化钠和硝酸钾固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液D.从含有少量氯化钠的硝酸钾饱和溶液中得到较多的硝酸钾晶体,通常可采用冷却热饱和溶液的方法3.将200g溶质质量分数为10%的蔗糖溶液倒掉一半,剩余的溶液溶质质量分数为()A.10%B.5%C.2.5%D.20%4.下列关于溶液的说法正确的是()A.通过加热蒸发的方法提高75%酒精的浓度B.SO42﹣、H+、OH﹣、Ba2+中能发生反应的离子有3对C.5g氢氧化钙溶于95g水中配制溶液,此溶液的溶质质量分数小于5%D.将50℃下的饱和KNO3溶液冷却至室温,硝酸钾固体析出,过滤后可得纯水和的硝酸钾固体5.食盐不仅是生活必需品,也是生产氯气和烧碱的重要原料。如图所示,20℃时在混合溶液中,随着氢氧化钠含量的变化,氯化钠达到饱和状态时其溶质质量分数的变化曲线。已知曲线上A、B、C、D四个点的坐标分别为A(0,26.5)、B(14.0,15.0)、C(18.8,11.7)、D(38.0,2.0)。下列说法正确的是()A.现有20℃时满足曲线上B点指标的溶液,可用蒸发水分降低氯化钠的质量分数B.氯化钠的溶解度随温度升高而减小C.C点处溶液中存在的粒子有Na+、Cl﹣、H2OD.20℃时,氯化钠在水中溶解度为26.5g6.下列有关溶液的说法中,正确的是()A.常温下将10mL饱和Ca(OH)2溶液加热到50℃,会使溶液由饱和溶液变为不饱和溶液B.将95gCaCl2溶液蒸干得到15g固体,则原溶液中CaCl2的质量分数为15%C.20℃时,50g水中溶解了18gNaCl,则20℃时NaCl的溶解度为36gD.从质量分数为10%的H2SO4溶液中取出10mL,则取出的10mLH2SO4溶液的质量分数仍为10%7.如表是NaCl、KNO3在不同温度时的溶解度:温度/℃102030405060溶解度/gNaCl35.836.036.336.637.037.3KNO320.93.1645.863.985.5110据此数据,下列说法正确的是()A.20℃时,将20gNaCl加入50g水中,得到70g溶液B.50℃时,KNO3溶液的溶质质量分数大于NaCl溶液的溶质质量分数C.降温时,KNO3溶液析出的固体质量大于NaCl溶液析出的固体质量D.NaCl和KNO3的溶解度曲线在20℃~30℃之间相交8.如图中不能正确反映题中所描述的变化事实的是()A.接近饱和的氯化钠溶液中加入氯化钠固体B.不饱和硝酸钾溶液升温C.一定量水中加入氯化钠D.加热蒸发稀盐酸9.氢氧化钙在80℃时的溶解度为xg,在20℃时的溶解度为yg。取20℃时的氢氧化钙饱和溶液,蒸发掉wg水后再恢复到20℃,其溶液中溶质的质量分数为z%,则下列关系式中正确的是()A.y>x,y>zB.x>y>zC.y<x,y<zD.x<y<z10.小陈查阅NH4Cl和NaCl的溶解度如表所示,对此理解正确的是()温度/℃01020304050NH4Cl溶解度/g29.433.337.241.445.850.4NaCl溶解度/g35.735.836.036.336.637.0A.NH4Cl的溶解能力比NaCl的溶解能力强B.20℃时饱和NaCl溶液质量分数为36%C.50℃时100克饱和NH4C1溶液,冷却到20℃将有13.2克晶体析出D.在10℃﹣20℃之间,会出现NaCl与NH4Cl溶解度相等的时刻11.图为M、N两种固体饱和溶液的溶质质量分数(C%)随温度(T)变化的曲线,下列说法正确的是()A.N的溶解度受温度的影响最大B.t℃时,M和N的溶解度均为40gC.t℃时,N的饱和溶液升温后仍是饱和溶液D.t℃时,M的饱和溶液中溶质与溶剂的质量比为2:512.下列说法正确的是()A.根据质量守恒定律,2gH2跟8gO2完全反应,可得到10H2OB.用含Fe2O385%的赤铁矿160t,理论上可生产100t含杂质4.8%的生铁C.各取10g镁粉和锌粉,分别与足量的盐酸完全反应,...