专 题 二 化 学 基 本 理 论【 复 习 指 南 】内容指要:本专题包括对元素周期表(长式)的结构(周期、族)的了解和元素周期律的实质的应用性掌握;能对化学反应速率的概念、反应速率的定量表示方法进行判断,能理解性甑别外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,明了化学平衡常数的含义,并能利用化学平衡常数进行简单的计算;能熟练运用电离和平衡原理分析和处理电解质溶液中的电离平衡、水解平衡及难溶电解质的溶解平衡及沉淀转化;能了解原电池和电解池工作原理,并能结合常见化学电源或新型电源写出电极反应和电池反应方程式
教材回眸:请认真阅读高中化学必修 2“第一章 物质结构 元素周期律”、必修 1“第三章 金属极其重要化合物、第四章 非金属及其重要化合物”、高中化学必修 2“第二章 第三节”、选修 4“第二章 化学反应速率和化学平衡”、高中化学选修 4“第三章 水溶液中的离子平衡”、高中化学必修 2“第二章 第二节 化学能与电能”、选修 4“第四章 电化学基础”等相关内容
专题重点:① 外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,尤其是对表格、数据等呈现方式的辨析;②结合实例书写和计算平衡常数;③常见化学电源或新型电源的电极反应和电池反应方程式的书写以及金属的电化学腐蚀原理及防腐措施的列举;④突破以元素推断为切入口,与具体物质、其它概念原理、实验、计算相融合的新题型
所需时间:共 7 课时,其中授课和课堂互动性练习 5 课时,习题讲评 2 课时
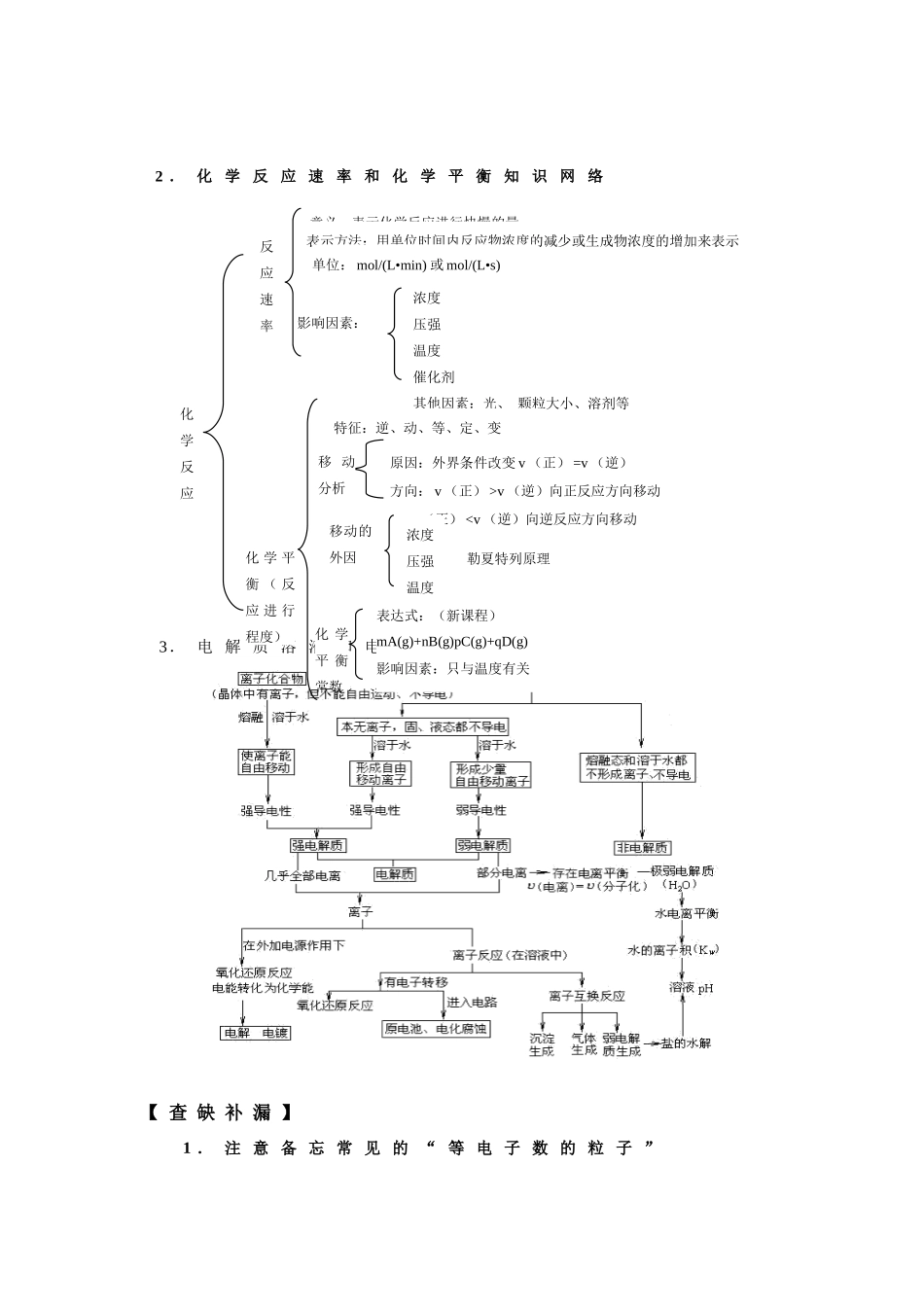
【 专 题 建 构 】 1 .原子结构和元素周期律知识的综合网络 2 . 化 学 反 应 速 率 和 化 学 平 衡 知 识 网 络 3. 电 解 质 溶 液 和 电 化 学 知 识 网 络【 查 缺 补 漏 】1 . 注 意 备 忘 常 见 的 “ 等 电 子 数 的 粒 子 ”意义:表示化学反应