2015 届高考化学大一轮复习 第七章 第一节 化学反应速率(含解析)第一节 化学反应速率1
了解化学反应速率的概念、反应速率的定量表示方法
了解催化剂在生产、生活和科学研究领域中的重要作用
理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,认识并能用相关理论解释其一般规律
了解化学反应速率的调控在生活、生产和科研领域中的重要作用
(中频) 化学反应速率1.概念2.化学反应速率与化学计量数关系对于已知反应 mA(g)+nB(g)pC(g)+qD(g),其化学反应速率可用不同的反应物或生成物来表示,当单位相同时,化学反应速率的数值之比等于化学计量数之比,即 v(A)∶v(B)∶v(C)∶v(D)=m ∶ n ∶ p ∶ q
3.反应速率的实验测定(1)原则:任何一种化学物质的浓度(或质量)有关的性质在测量反应速率时都可以加以利用
(2)测定的角度① 直接观察的某些性质,如放出气体的体积和体系压强;② 依靠科学仪器测量的性质,如颜色深浅、光的吸收、光的发射、导电能力等;③ 溶液中利用颜色深浅与显色物质浓度间的正比关系,测量反应速率
影响化学反应速率的因素1.内因反应物本身的性质是主要因素
如相同条件下 Mg、Al 与稀盐酸反应的速率大小关系为Mg>Al
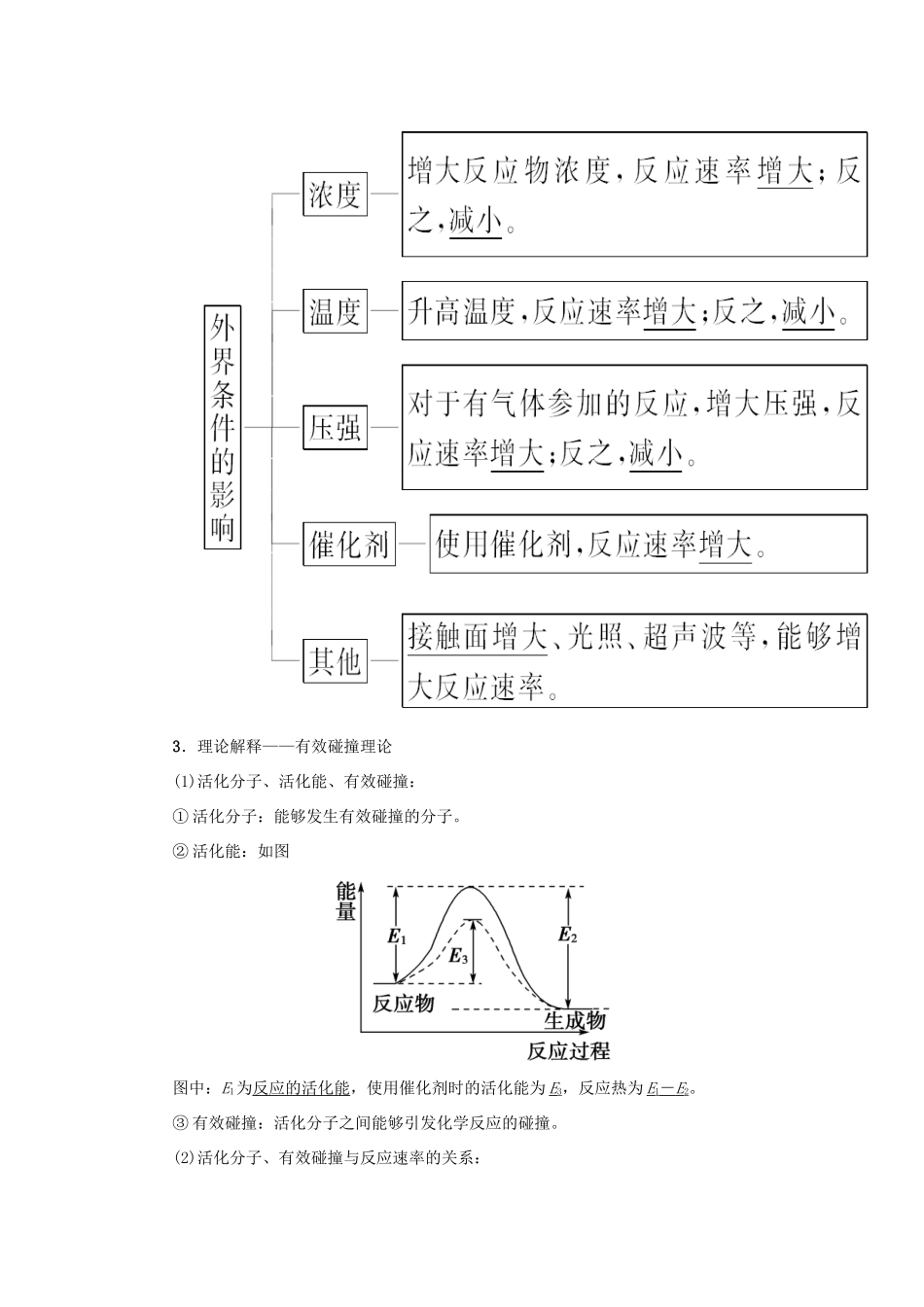
2.外因3.理论解释——有效碰撞理论(1)活化分子、活化能、有效碰撞:① 活化分子:能够发生有效碰撞的分子
② 活化能:如图图中:E1为反应的活化能,使用催化剂时的活化能为 E3,反应热为 E1- E 2
③ 有效碰撞:活化分子之间能够引发化学反应的碰撞
(2)活化分子、有效碰撞与反应速率的关系:1.易误诊断(正确的打“√”,错误的打“×”)
(1)对于 C(s)+H2O(g)H2(g)+CO(g)反应 v(C)=v(H2O)( )(2)化学反应速率一定随着时间的延长而减小( )