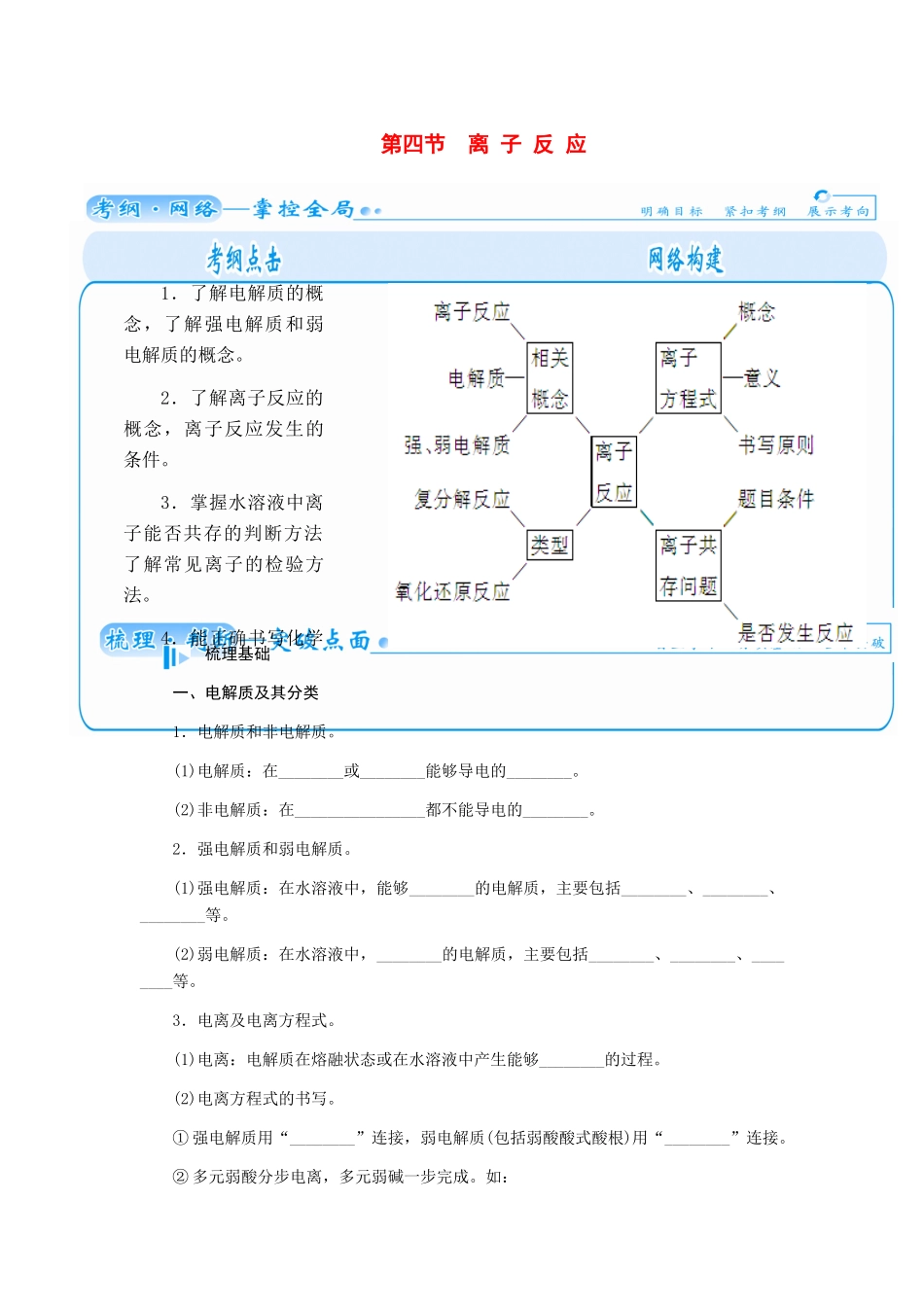
第四节 离 子 反 应 梳理基础一、电解质及其分类1.电解质和非电解质。(1)电解质:在________或________能够导电的________。(2)非电解质:在________________都不能导电的________。2.强电解质和弱电解质。(1)强电解质:在水溶液中,能够________的电解质,主要包括________、________、________等。(2)弱电解质:在水溶液中,________的电解质,主要包括________、________、________等。3.电离及电离方程式。(1)电离:电解质在熔融状态或在水溶液中产生能够________的过程。(2)电离方程式的书写。① 强电解质用“________”连接,弱电解质(包括弱酸酸式酸根)用“________”连接。② 多元弱酸分步电离,多元弱碱一步完成。如:1.了解电解质的概念,了解强电解质和弱电解质的概念。2.了解离子反应的概念,离子反应发生的条件。3.掌握水溶液中离子能否共存的判断方法了解常见离子的检验方法。4.能正确书写化学方程式和离子方程式,Na2SO4____________________,H2CO3________________,__________________,Fe(OH)3____________________。③ 酸式盐。强酸酸式盐完全电离,一步到底。NaHSO4在水溶液中的电离方程式为__________________。NaHSO4在熔融状态下的电离方程式为______________。多 元 弱 酸 酸 式 盐 , 第 一 步 完 全 电 离 , 其 余 的 部 分 电 离 , 如 :NaHCO3________________________________。二、离子反应1.概念:有________参加的化学反应,电解质溶液之间发生的反应都是离子反应。2.实质:使溶液中的离子浓度________。3.条件:有________或________或____________生成或离子(或分子)有电子________。4.离子方程式。(1)概念:用________________来表示离子反应的式子。(2)书写步骤(以 CaCO3与盐酸的反应为例)。(3)意义。表示符合此离子反应方程式的一类离子反应。例如,离子方程式 H++OH-===H2O 表示________________________________。答案:梳理基础一、1.(1)水溶液里 熔融状态下 化合物 (2)水溶液里和熔融状态下 化合物2.(1)全部电离 强酸 强碱 大多数盐 (2)部分电离 弱酸 弱碱 水 [来源:Zxxk.Com]3.(1)自由移动离子 (2)①=== ② Na2SO4 === 2Na ++SO42- H2CO3HCO3-+H + HCO3-CO32-+H + Fe(OH)3Fe3 ++3OH - ③ NaHSO4 === Na++H++SO NaHSO4===Na++HSO NaHCO3===Na++HCO, HCOH++CO二、1.离子 2....