江苏省响水中学 2014 届高三化学一轮复习学案:第 44 课时 离子浓度的比较 2【考纲要求】熟悉高考原题,并比较溶液中离子浓度的大小【考点分析】1.常温下,向 25mL0
1mol L-1 NaOH∙溶液中逐滴加入 0
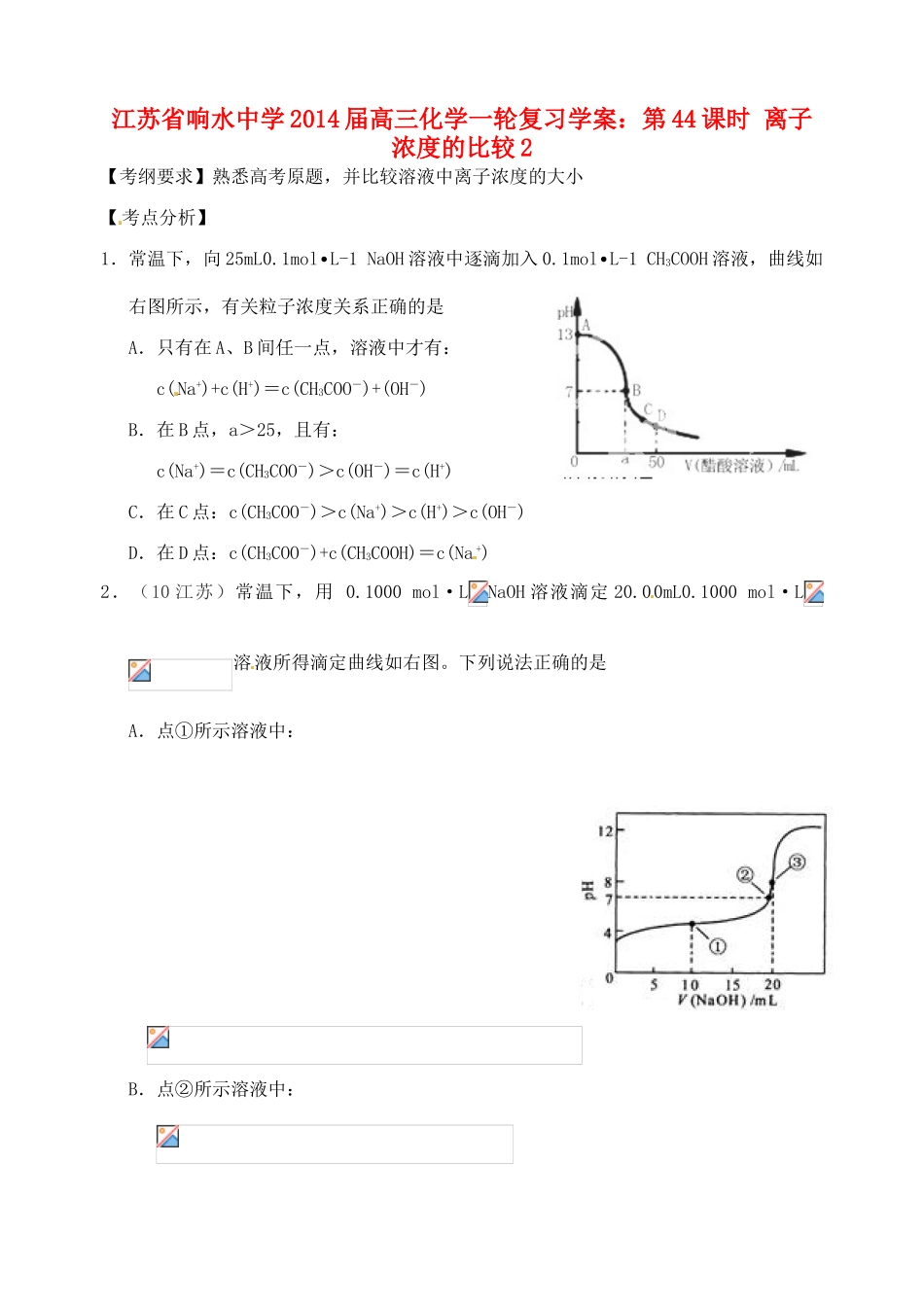
1mol L-1 CH∙3COOH 溶液,曲线如右图所示,有关粒子浓度关系正确的是 A.只有在 A、B 间任一点,溶液中才有:c(Na+)+c(H+)=c(CH3COO-)+(OH-) B.在 B 点,a>25,且有:c(Na+)=c(CH3COO-)>c(OH-)=c(H+)C.在 C 点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)D.在 D 点:c(CH3COO-)+c(CH3COOH)=c(Na +)2.(10 江苏)常温下,用 0
1000 mol·LNaOH 溶液滴定 20
1000 mol·L溶液所得滴定曲线如右图
下列说法正确的是A.点①所示溶液中:B.点②所示溶液中:C.点③所示溶液中:D.滴定过程中可能出现:3.(09 江苏)下列溶液中微粒的物质的量浓度关系正确的是A . 室 温 下 , 向 0
01溶 液 中 滴 加溶 液 至 中 性 :B.0
1溶液:C.溶液:D.25℃时,、浓度均为 0
1的混合溶液:4.(11 江苏)下列有关电解质溶液中微粒的物质的量浓度关系正确的是A
1mol·L-1NaHCO3溶液中:c(Na+) c(HCO3+) c(CO32-) c(H2CO3)B
1mol·L-1Na2CO3溶液中:c(OH-)- c(H+)= c(HCO3-)+2c(H2CO-)C
2 mol·L-1NaHCO3溶液中加入等体积 0
1mol·L-1NaOH 溶液:c(Na+)= c(CH3COO-)> c(CH3COOH)> c(H+)= c(OH-)D
常温下,CH3COON