河南省焦作市沁阳一中 2014 高中化学 第二节 几种重要的金属化合物导学案(第二课时)新人教版必修 1【学习目标】1. 掌握 Al2O3 、Al(OH)3的两性2. 掌握 Al(OH)3的实验室制备方法【学习重点】 Al2O3、Al(OH)3的两性【学习难点】 Al(OH )3的实验室制备及两性探究【自主学习】阅读教材 58-59 页内容,回答下列问题1
氧化铝(1)物理性质:
(2)用途:
(3)化学性质:写出下列反应的化学方程式,并改成离子方程式
Al2O3和 HCl , Al2O3和 NaOH , 结论:Al2O3既可以与酸反应又可以与强碱反应且都生成盐和水,因此 Al2O3是 氧化物
思考:为了除去 MgO 中的少量杂质 Al2O3,可以选用什么试剂
氢氧化铝(1)制备实验室没有现存的 Al(OH)3,我们如何制备
现提供如下试剂:稀 HCl、稀氨水、NaOH 溶液和 Al2(SO4)3溶液,请讨论制备的原理和相关反应的方程式
小组实验:(P58 实验 3—7) 化学方程式 离子方程式 (2)物理性质 (3)化学性质小组实验:(P58 实验 3—8) ①与酸的反应 ②与强碱的反应 结论:Al(OH)3 既 可以与酸反应,又可以与强碱反应,且都生成盐和水
因此 Al(OH)3是 氢氧化物
学与问:为什么常用氨水与硫酸铝溶液反应制取氢氧化铝,而不用氢氧化钠溶液呢
请写出硫酸铝溶液与过量的氢氧化钠溶液反应的离子方程式
有一种药叫胃舒平,你知道它的作用吗
你知道它的成分是什么
③Al(OH)3的不稳定性Al(OH)3受热分解的化学方程式 讨论:哪些金属氢氧化物热稳定性差
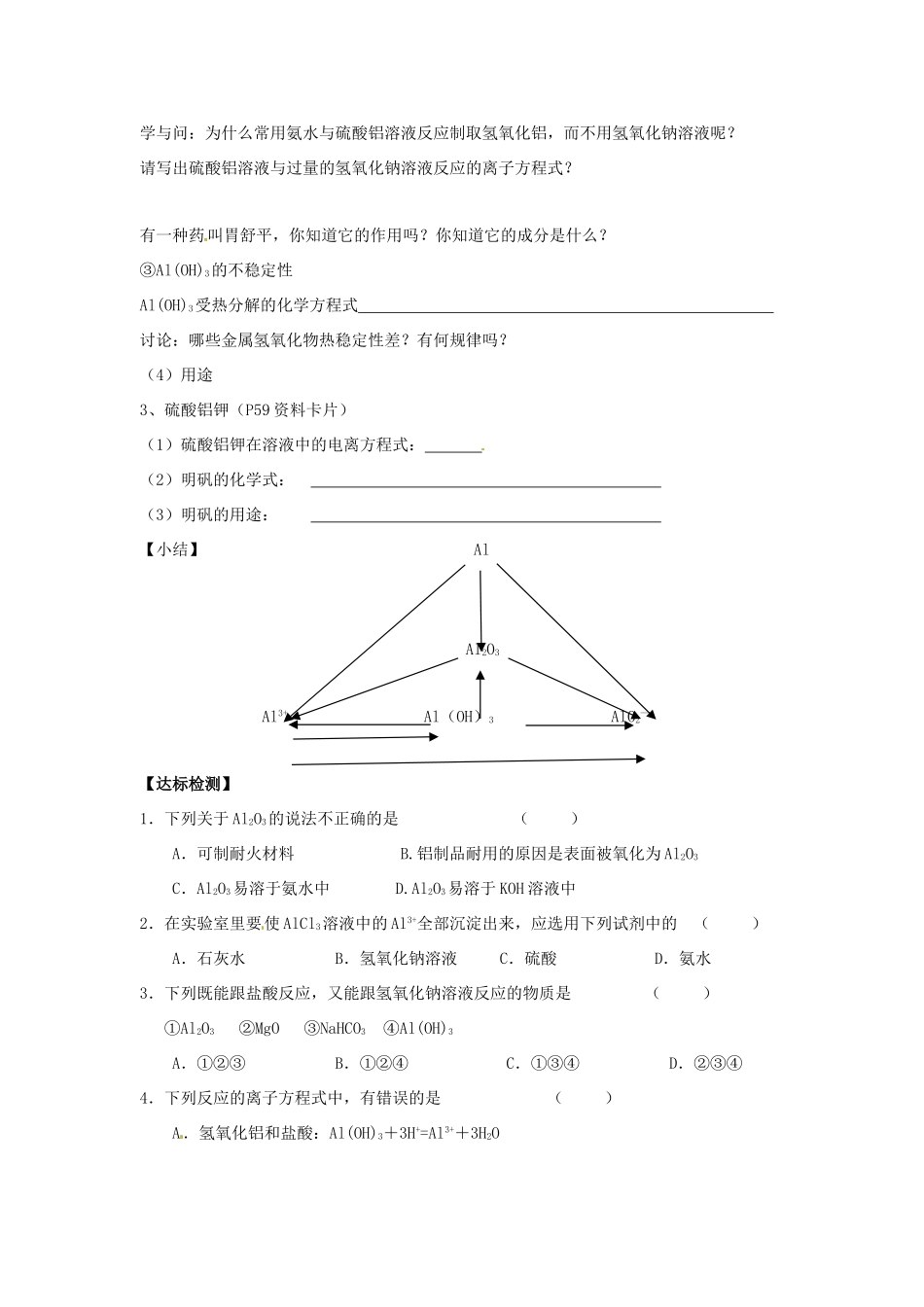
(4)用途 3、硫酸铝钾(P59 资料卡片)(1)硫酸铝钾在溶液中的电离方程式: (2)明矾的化学式: (3)明矾的用途: 【小结】 Al Al2O3Al3+ Al(OH)3 AlO