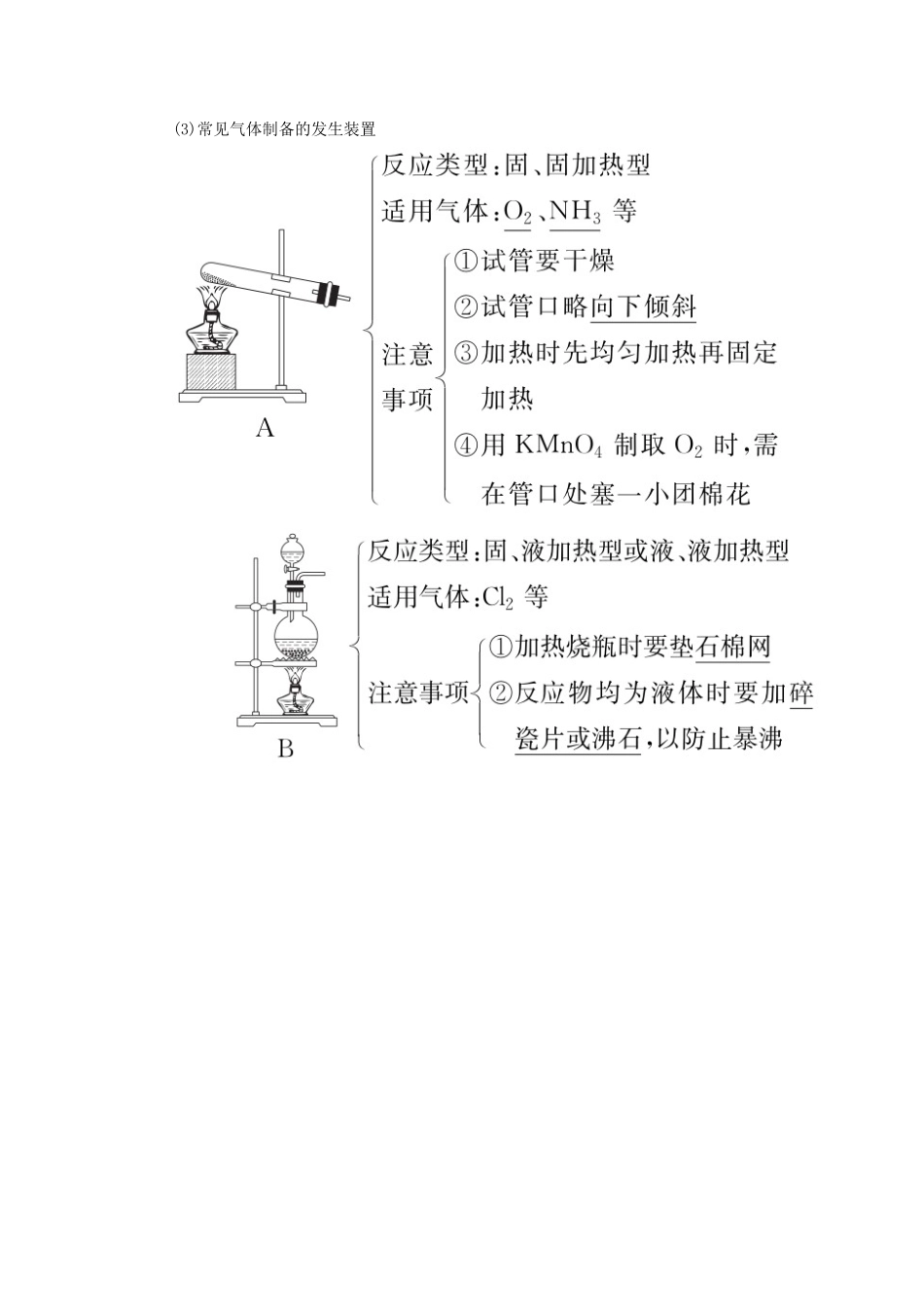
专题二十五 实验方案的设计与评价考纲展示 命题探究1 气体物质的制备实验(1)气体实验的操作顺序① 安装顺序a.由下到上(如制氯气的发生装置安装顺序是:放铁架台→摆酒精灯→固定铁圈→放置石棉网→固定圆底烧瓶)
b.从左到右(如制氯气:发生装置→净化装置→收集装置→吸收装置)
c.先塞后定(把带导管的胶塞在烧瓶固定前塞好,以免烧瓶固定后因不宜用力而塞不紧或因用力过猛而损坏仪器)
② 加试剂顺序固体先放入,液体后滴加(即先固后液)
③ 其他操作顺序先检验气密性,后装入药品(便于在装置漏气时进行调整或更换仪器),最后点燃酒精灯(所有准备工作完毕后);在连接导管时,应长进短出;量气装置的导管应短进长出;干燥管应大口进,小口出
(2)常见气体制备的反应原理气体反应原理O22KMnO4=====K2MnO4+MnO2+O2↑2KClO3=====2KCl+3O2↑2Na2O2+2H2O===4NaOH+O2↑2H2O2=====2H2O+O2↑续表气体反应原理H2较活泼金属(如 Zn、Fe)与稀强酸(如稀硫酸、盐酸,但勿用硝酸或浓硫酸)的置换反应CO2CaCO3+2HCl===CaCl2+CO2↑+H2OCl2MnO2+4HCl(浓)=====MnCl2+Cl2↑+2H2O2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2ONH32NH4Cl+Ca(OH)2=====2NH3↑+2H2O+CaCl2(实验室亦常用浓氨水中加 NaOH 固体来制取少量 NH3)SO2无水 Na2SO3粉末与中等浓度硫酸进行复分解反应:Na2SO3+H2SO4===Na2SO4+H2O+SO2↑NO2Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2ONO3Cu+8HNO3(稀)=====3Cu(NO3)2+2NO↑+4H2OC2H4CH3CH2OH――→CH2===CH