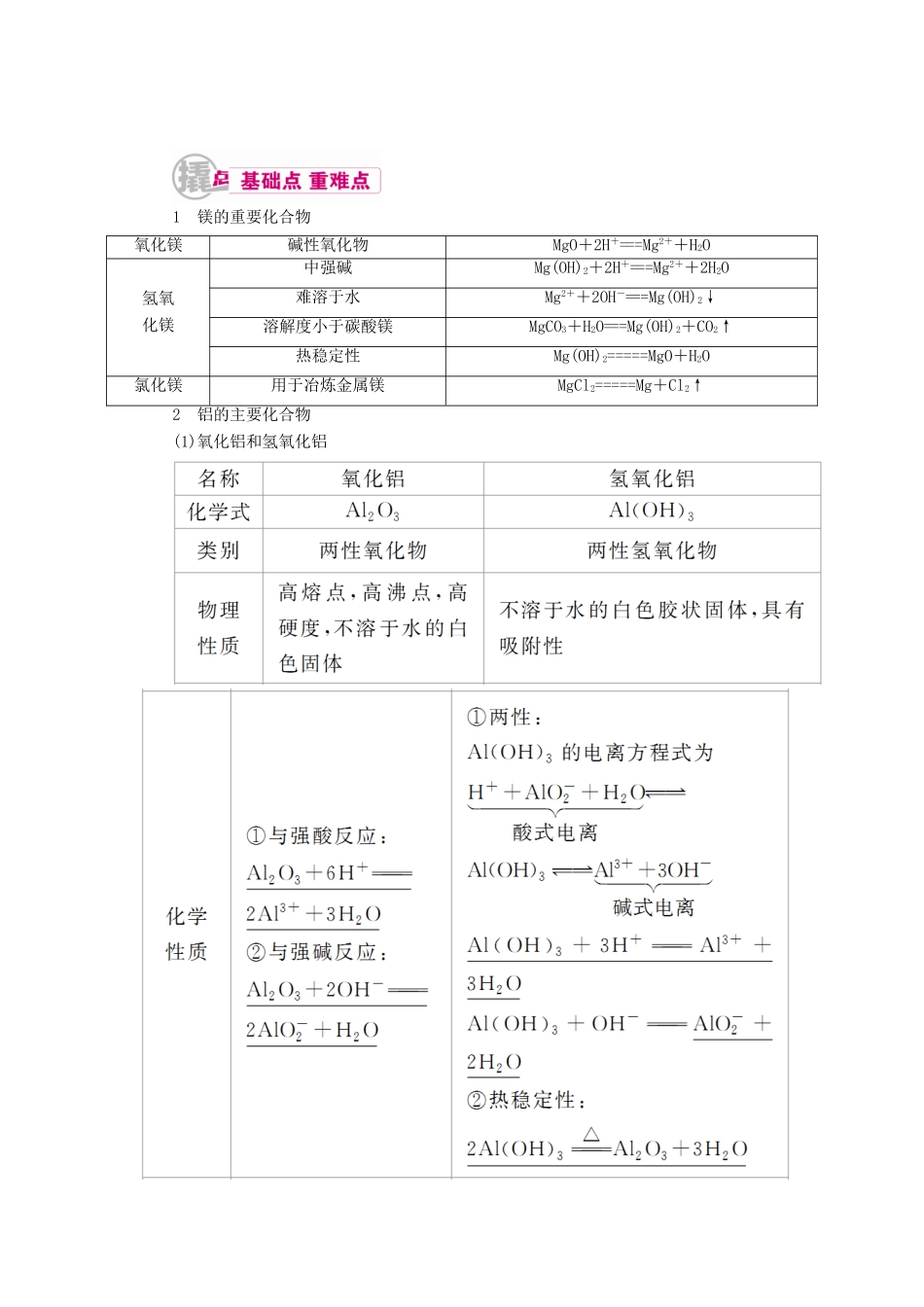
1 镁的重要化合物氧化镁碱性氧化物MgO+2H+===Mg2++H2O氢氧化镁中强碱Mg(OH)2+2H+===Mg2++2H2O难溶于水Mg2++2OH-===Mg(OH)2↓溶解度小于碳酸镁MgCO3+H2O===Mg(OH)2+CO2↑热稳定性Mg(OH)2=====MgO+H2O氯化镁用于冶炼金属镁MgCl2=====Mg+Cl2↑2 铝的主要化合物(1)氧化铝和氢氧化铝(2)复盐——硫酸铝钾① 复盐定义:由两种不同的金属离子(或 NH)与一种酸根离子组成的盐叫复盐。② 明矾明矾的化学式为 KAl(SO4)2·12H2O,可溶于水,电离方程式为 KAl(SO4)2===K++Al3++2SO。水溶液的 pH<7(填“>”“<”或“=”),原因是 Al3++3H2OAl(OH)3+3H+。明矾可用于净水,其原因是 Al 3 + 水解产生 Al(OH) 3 胶体, Al(OH) 3 胶体可以和悬浮于水中的泥沙形成絮状不溶物而沉降下来,使水澄清。学霸巧学卡 对镁、铝化合物的深层解析(1)由于 Mg(OH)2 的溶解度比 MgCO3 的小,故水垢的主要成分中是 Mg(OH)2,而非MgCO3。(2)Al2O3、Al(OH)3只与强酸、强碱溶液反应,与氨水和碳酸溶液不反应。(3)Al3+只能存在于酸性溶液中,AlO 只能存在于碱性溶液中。若将分别含 Al3+和 AlO的盐溶液混合,发生反应:Al3++3AlO+6H2O===4Al(OH)3↓。(4)Al2O3、Al(OH)3是中学阶段接触的唯一与碱反应的金属氧化物和氢氧化物,经常应用到除杂、计算题中,所以一定要熟记这两个反应的离子方程式。(5)明矾净水只能除去水中的悬浮杂质,不能杀菌消毒,与氯气消毒原理不同。1.思维辨析(1)在加热情况下利用氢气还原氧化铝的方法得到金属铝。( )(2)将 Al(OH)3沉淀转入蒸发皿中,加足量稀硫酸,加热蒸干得无水 Al2(SO4)3固体。( )(3)将 NaOH 溶液缓慢滴入 Al2(SO4)3溶液中至过量,最终观察到有沉淀生成。( )(4)日用铝制品表面覆盖着氧化膜对内部金属起保护作用。( )(5)Al2O3的熔点很高,可用作耐高温材料。( )(6)明矾水解形成的 Al(OH)3胶体能吸附水中的悬浮物,可用于对水的杀菌、消毒。( )答案 (1)× (2)√ (3)× (4)√ (5)√ (6)×2.将等体积的 AlCl3溶液和 NaOH 溶液混合后,沉淀物中含铝元素的物质的量与溶液中含铝元素的物质的量相等,则原 AlCl3溶液与 NaOH 溶液的物质的量浓度之比是 ( )A.1∶3 B.2∶5C.1∶4 D.2∶7答案 D解析 设 AlCl3 和 NaOH 的物质的量分别为 a、b。当 NaOH 少量时,铝元素以 Al3+和Al(OH)3形式存在,×3=b,a∶b=2∶3;当 NaOH 过量时,铝元素以 Al(OH...