配合物与沉淀——溶解平衡一
实验目得1. 加深理解配合物得组成与稳定性
了解配合物形成时特征2. 加深理解沉淀—溶解平衡与溶度积得概念
掌握溶度积规则及其应用3. 初步学习利用沉淀反应与配位溶解得方法,分离常见混合阳离子4. 学习电动离心机得使用与固—液分离操作二
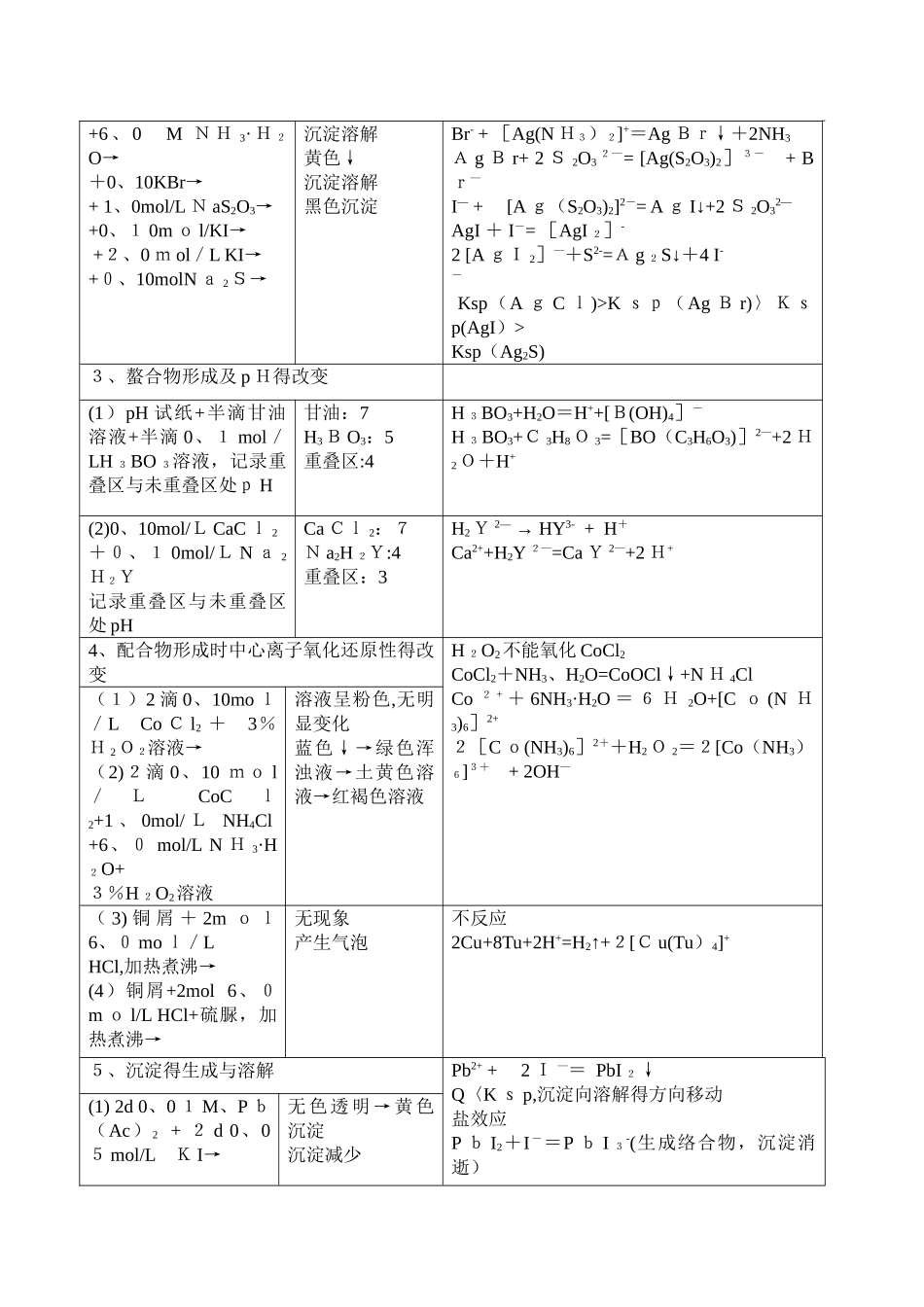
实验内容步骤现象反应方程式、解释或结论1、配合物得形成与颜色变化Fe3+ + nSCN—=[Fe(S C N)n]3-n [F e(SC N)n]3-n + 6 F- = [Fe F 6]3-+n S CN-Cu2++4NH 3 = [Cu(NH3)4]2+不反应SO 4 2— + Ba 2+=BaSO4↓无水乙醇与水互溶使[Cu(N H3)4] S O 4溶解度减小析出NiSO4+6NH 3 = Ni(NH 3)6S O4N i2 + +2NH3+2dmg = [Ni(dmg ) 2 ] ↓ +2NH4+(1)2 d 0、1 mo l/L F e Cl3 + 1d0、10mol/LK S C N→+ 0、5mol/L N aF→(3 ) 几 滴0 、 10mol/LCu S O4+ 6、0 mol/L NH3·H 2O至过量→+ 2、0mol/LNa O H→+ 0 、 10mol/LBa Cl2→少量无水乙醇→(4))2d 0、1 0mol/LN iSO4 + 6m o l 、 L N H3·H2O→+ 2d 丁二酮肟试剂→血红色变无色浅蓝沉淀变为深蓝色溶液无现象出现白色沉淀蓝色沉淀析出溶液由绿色变为蓝色出现鲜红色沉淀2、配合物形成时难溶物溶解度得改变Cl- + Ag+ = AgCl↓ (白)AgC l+2N H 3·H2O=[A g(N H3)2]++Cl—+2 H 2O[Ag(NH3)2]++2 H++Cl-=AgCl↓+2NH4+( 1 )0 、 10 m o l /LNaCl + 0 、 10m o