溶液组成的表示方法盐加的越多,溶液越咸,此时浓度越大
溶液的浓与稀是指溶质含量的相对多少,它不能准确的表明一定量的溶液中所含溶质的多少
怎样确切的表示一定量的溶液中含多少溶质呢
一、溶质的质量分数溶质质量溶液质量×100%溶质的质量分数=或=溶质质量溶质质量 + 溶剂质量×100%定义式:定义:溶质的质量与溶液的质量之比
想一想:上述实验配制的溶液中氯化钠的质量分数是多少
二、溶液中溶质的质量分数计算 例 1 :从一瓶氯化钾溶液中取出 20 克溶液,蒸干后得到2
8 克氯化钾固体
试确定这瓶溶液中溶质的质量分数
这瓶溶液中溶质的质量分数为:溶质质量溶液质量×100%解:溶质的质量分数=答:这瓶溶液中氯化钾的质量分数为 14%
8g20g ×100%= 14%例 2 :把 50g98% 的硫酸稀释成 20% 的硫酸 , 需要水多少克
解:溶液稀释前后,溶质的质量不变
稀释前、后溶质的质量为: 50g× 98%=49g溶质质量溶液质量溶质的质量分数=溶质质量溶质的质量分数溶液质量=需要水的质量是: 49g20%- 50g = 195g例 3 :配制 500mL20% 的硫酸需要 98% 的硫酸多少毫升
解:查硫酸密度和溶质质量分数对照表得出: 20% 的硫酸的密度为 1
14g/cm3 , 98% 的硫酸的密度为 1
84g/cm3
设:需 98% 的硫酸的体积为 x
因被稀释的溶液里溶质的质量在稀释前后不变,又因为:质量 = 体积 × 密度可以列出下式:x × 1
84g/cm3 × 98%=500 cm3 × 1
14g/cm3 × 20%稀释前溶液中含 H2SO4 的质量稀释后溶液中含 H2SO4 的质量x = 63
2 cm3答:配制 500mL20% 的硫酸需要 63
2mL98% 的硫酸
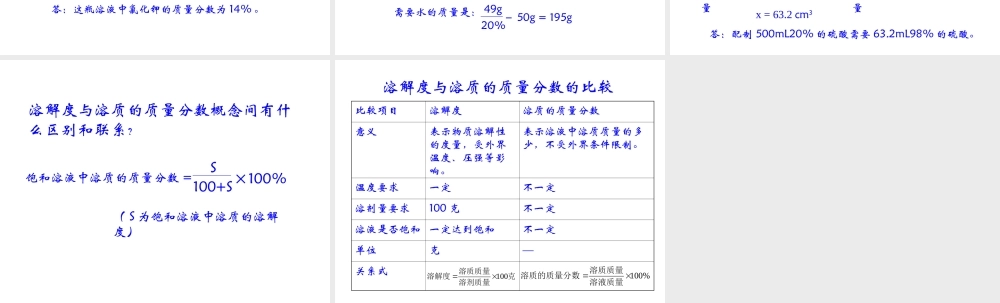
溶解度与溶质的质量分数概念间有什么区别和联系
( S 为饱和溶