题组36以陌生无机物制备流程为载体的综合题专练1
2019年为门捷列夫发现元素周期律150周年
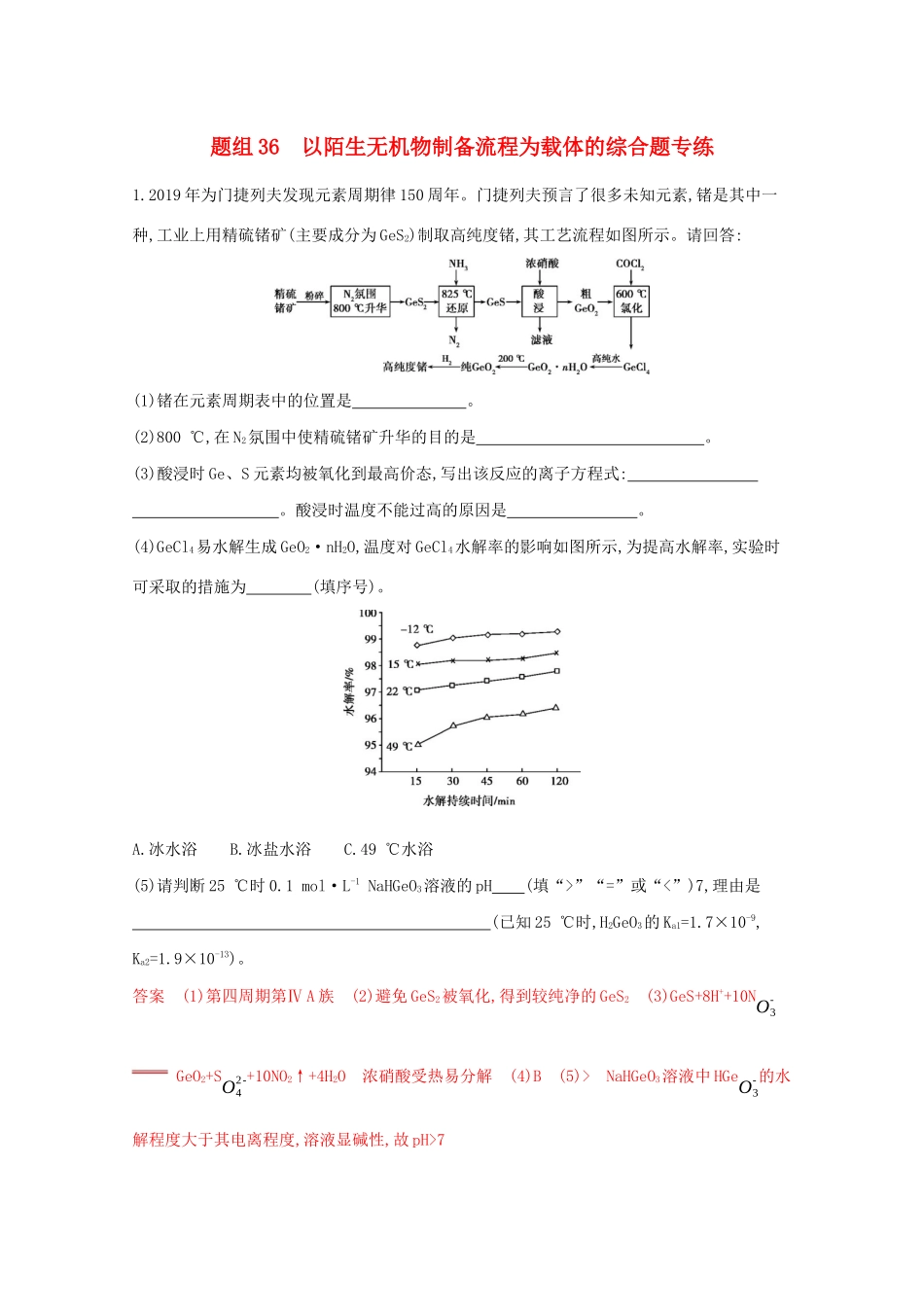
门捷列夫预言了很多未知元素,锗是其中一种,工业上用精硫锗矿(主要成分为GeS2)制取高纯度锗,其工艺流程如图所示
请回答:(1)锗在元素周期表中的位置是
(2)800℃,在N2氛围中使精硫锗矿升华的目的是
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:
酸浸时温度不能过高的原因是
(4)GeCl4易水解生成GeO2·nH2O,温度对GeCl4水解率的影响如图所示,为提高水解率,实验时可采取的措施为(填序号)
49℃水浴(5)请判断25℃时0
1mol·L-1NaHGeO3溶液的pH(填“>”“=”或“NaHGeO3溶液中HGeO3-的水解程度大于其电离程度,溶液显碱性,故pH>7解析(1)Ge在元素周期表中位于第四周期第ⅣA族
(2)根据题干信息可知,在N2氛围中使精硫锗矿升华的目的是避免GeS2被氧化,得到较为纯净的GeS2
(3)浓硝酸酸浸GeS时,Ge、S元素均被氧化到最高价态,则生成GeO2、SO42-,NO3-被还原为二氧化氮气体,离子方程式为GeS+8H++10NO3-GeO2+SO42-+10NO2↑+4H2O;浓硝酸受热易分解,故酸浸时温度不能过高
(4)GeCl4易水解生成GeO2·nH2O,根据题图知,温度较低时水解率较高,为提高水解率,可选用冰盐水浴
(5)已知25℃时H2GeO2的Ka1=1
7×10-9,Ka2=1
9×10-13,NaHGeO3的水解常数Kh=KwKa1=11
7×10-5>Ka2(1
9×10-13),即NaHGeO3溶液中HGeO3-的水解程度大于其电离程度,溶液显碱性,故pH>7
锑(Sb)及其化合物在工业上有许多用途
以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、C