专练七盖斯定律的应用及热化学方程式的书写与判断题型狂练1.(2013·福建理综,11)某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO
其过程如下:mCeO2――――→(m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+xCO2―――→mCeO2+xH2+xCO下列说法不正确的是()
A.该过程中CeO2没有消耗B.该过程实现了太阳能向化学能的转化C.右图中ΔH1=ΔH2+ΔH3D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-===CO32-+2H2O解析由盖斯定律可知ΔH1=-(ΔH2+ΔH3),C项错
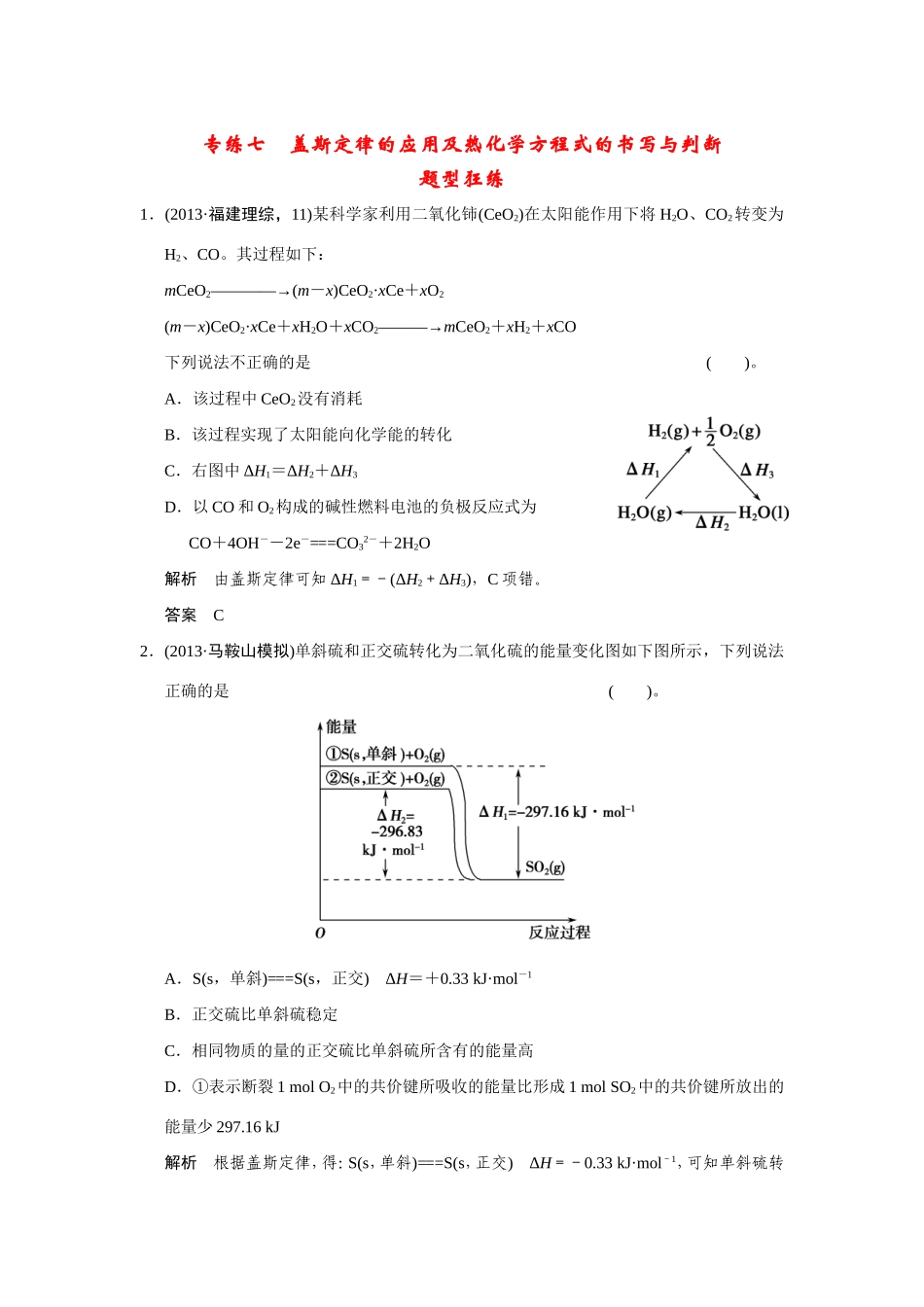
答案C2.(2013·马鞍山模拟)单斜硫和正交硫转化为二氧化硫的能量变化图如下图所示,下列说法正确的是()
A.S(s,单斜)===S(s,正交)ΔH=+0
33kJ·mol-1B.正交硫比单斜硫稳定C.相同物质的量的正交硫比单斜硫所含有的能量高D.①表示断裂1molO2中的共价键所吸收的能量比形成1molSO2中的共价键所放出的能量少297
16kJ解析根据盖斯定律,得:S(s,单斜)===S(s,正交)ΔH=-0
33kJ·mol-1,可知单斜硫转化为正交硫时要放出热量,正交硫的能量要低,较稳定,故A项错误、B项正确;相同物质的量的正交硫应该比单斜硫所含有的能量低,C项错误;①表示断裂1molS(s,单斜)和1molO2(g)中的共价键所吸收的能量比形成1molSO2(g)中的共价键所放出的能量少297
16kJ,D项错误
答案B3.(2013·北京大兴期末,19)由金红石(TiO2)制取单质Ti涉及的步骤为:TiO2―→TiCl4――→Ti已知:①C(s)+O2(g)===CO2(g)ΔH1=-393
5kJ·mol-1②2CO(g)+O2(g)===2CO2(g)ΔH2=-566kJ·mol-