课时32难溶电解质的溶解平衡及时巩固课堂评价1
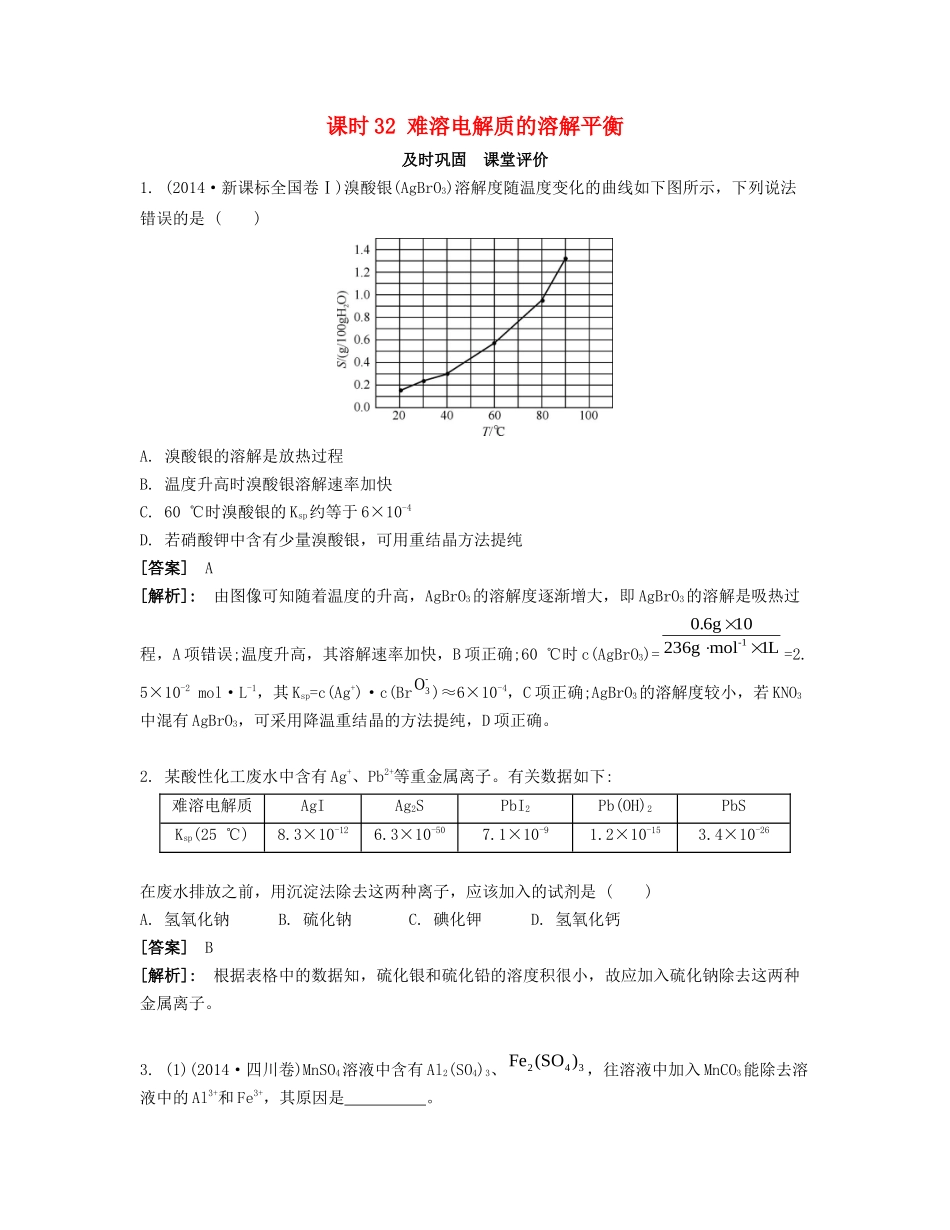
(2014·新课标全国卷Ⅰ)溴酸银(AgBrO3)溶解度随温度变化的曲线如下图所示,下列说法错误的是()A
溴酸银的溶解是放热过程B
温度升高时溴酸银溶解速率加快C
60℃时溴酸银的Ksp约等于6×10-4D
若硝酸钾中含有少量溴酸银,可用重结晶方法提纯[答案]A[解析]:由图像可知随着温度的升高,AgBrO3的溶解度逐渐增大,即AgBrO3的溶解是吸热过程,A项错误;温度升高,其溶解速率加快,B项正确;60℃时c(AgBrO3)==2
5×10-2mol·L-1,其Ksp=c(Ag+)·c(Br)≈6×10-4,C项正确;AgBrO3的溶解度较小,若KNO3中混有AgBrO3,可采用降温重结晶的方法提纯,D项正确
某酸性化工废水中含有Ag+、Pb2+等重金属离子
有关数据如下:难溶电解质AgIAg2SPbI2Pb(OH)2PbSKsp(25℃)8
3×10-126
3×10-507
1×10-91
2×10-153
4×10-26在废水排放之前,用沉淀法除去这两种离子,应该加入的试剂是()A
氢氧化钙[答案]B[解析]:根据表格中的数据知,硫化银和硫化铅的溶度积很小,故应加入硫化钠除去这两种金属离子
(1)(2014·四川卷)MnSO4溶液中含有Al2(SO4)3、,往溶液中加入MnCO3能除去溶液中的Al3+和Fe3+,其原因是
6g10236gmol1L-3O243Fe(SO)(2)已知室温下BaSO4的Ksp=1
1×10-10,欲使溶液中c(S)≤1
0×10-6mol·L-1,应保持溶液中c(Ba2+)≥mol·L-1
(3)已知常温下Mg(OH)2的Ksp=1
8×10-11,若溶液中c(OH-)=3
0×10-6mol·L-1,则溶液中c(Mg2+)=