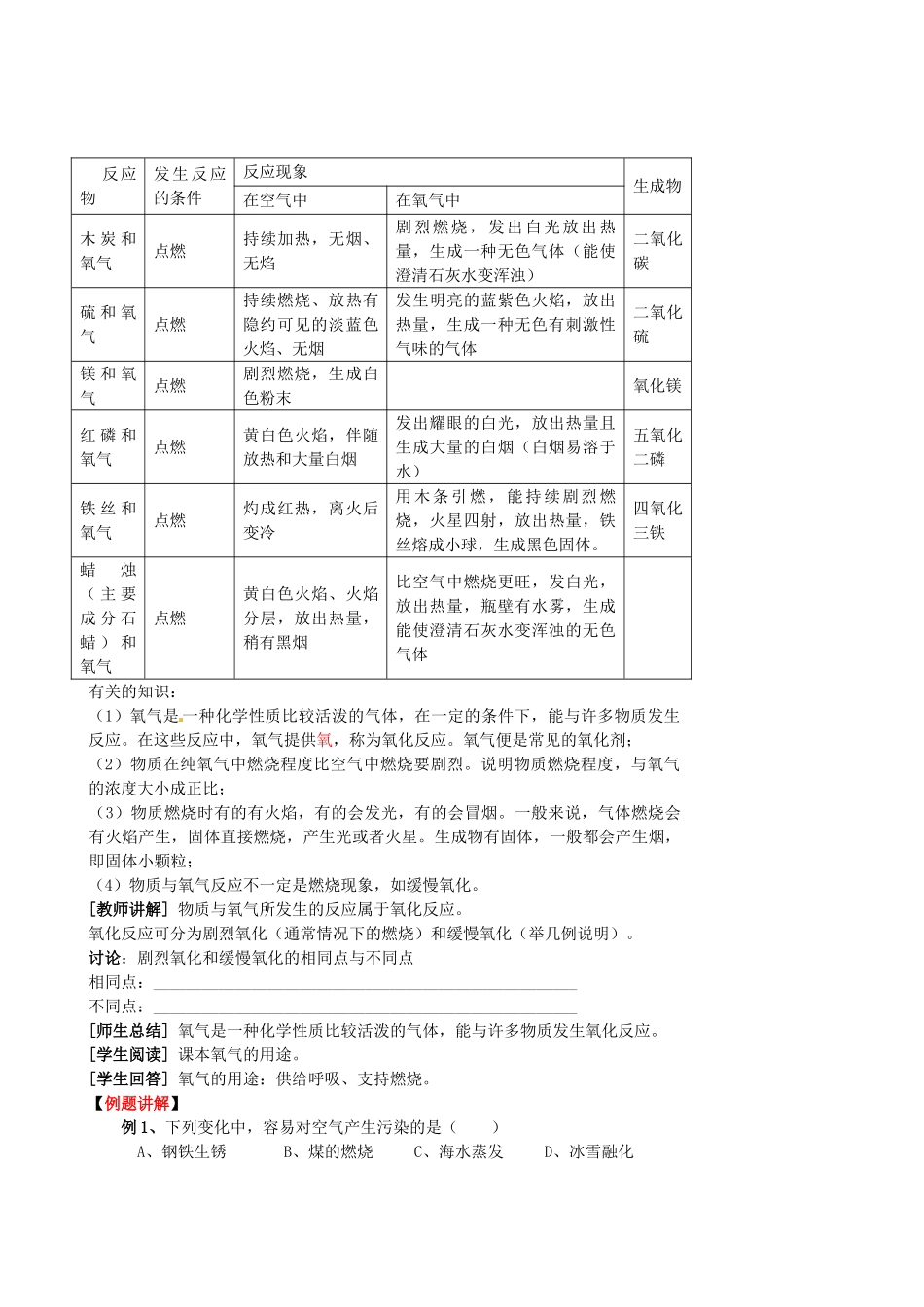
第二章第一节性质活泼的氧气第一课时:氧气的性质与用途教学目标:1、知识与能力:1.认识氧气的主要物理性质;2.观察和描述木炭、铁丝、蜡烛等在氧气中燃烧的现象,从中归纳出氧气的化学性质;3.了解氧气的主要用途、氧气与人类的密切关系;4.了解氧气的工业制法,学习实验室制备氧气的原理、装置和操作,一般性了解两套装置的区别。2、过程与方法:学会观察、叙述并记录有关化学实验的现象,并得出有关结论。3、情感、态度与价值观:向学生渗透物质的性质决定物质的用途,用途又体现性质的辩证观点。学习重点与难点:氧气的化学性质和获得教学用具:仪器:集气瓶(5个装有氧气)、燃烧匙、酒精灯等。药品:木炭、硫粉、红磷、红铁丝、蜡烛,石灰水、氧气。其它:火柴。课时安排:3课时课堂学习:一、引入:地球上的一切生命体都离不开氧气。[问题情景]1.为什么各种生物在消耗氧气,而空气中的氧气含量却能几乎保持恒定?2.你已知道氧气的哪些物理性质与化学性质?3.有什么事实能证明自然界的水中溶有氧气?[学生交流]同桌的同学间互相讨论与交流,然后回答问题。(教师进行相关的整理:将学生所描述的有关性质列于黑板上)二、师生互动:[教师引导]观察身边的空气,并阅读课本33—34页的部分内容。[师生整理]一、氧气的物理性质色、态、味、溶解性、密度(与空气比较)、三态变化(在通常情况下是无色无味气态,不易溶于水,密度大于空气,在一个标准大气压—183℃时氧气变为淡蓝色液体;—218.4℃变为淡蓝色雪花状固体。)[问题情景]大家知道,很多物质可以在空气中燃烧,你知道是空气中的什么成分支持这些物质燃烧?请举例说明。[实验演示]少量硫在空气和氧气中燃烧[师生整理]硫在空气和氧气中燃烧的现象和反应(产生微弱的淡蓝色火焰,有刺激性气味的气体产生)[教师设疑]硫在氧气中燃烧比在空气中更旺,那么能在空气中燃烧的木炭、蜡烛在氧气中燃烧的情况又是怎样呢?[实验演示]木炭、蜡烛在空气和氧气中燃烧。[师生整理]木炭、蜡烛在空气和氧气中燃烧的现象和反应[教师设疑]1.铁丝在空气中燃烧吗?2.铁丝在纯氧中又能否燃烧?[实验演示]铁丝在氧气中的燃烧[学生整理]将以上实验现象和反应的文字表达式进行整理,填入课本35页表格中。反应物发生反应的条件反应现象生成物在空气中在氧气中木炭和氧气点燃持续加热,无烟、无焰剧烈燃烧,发出白光放出热量,生成一种无色气体(能使澄清石灰水变浑浊)二氧化碳硫和氧气点燃持续燃烧、放热有隐约可见的淡蓝色火焰、无烟发生明亮的蓝紫色火焰,放出热量,生成一种无色有刺激性气味的气体二氧化硫镁和氧气点燃剧烈燃烧,生成白色粉末氧化镁红磷和氧气点燃黄白色火焰,伴随放热和大量白烟发出耀眼的白光,放出热量且生成大量的白烟(白烟易溶于水)五氧化二磷铁丝和氧气点燃灼成红热,离火后变冷用木条引燃,能持续剧烈燃烧,火星四射,放出热量,铁丝熔成小球,生成黑色固体。四氧化三铁蜡烛(主要成分石蜡)和氧气点燃黄白色火焰、火焰分层,放出热量,稍有黑烟比空气中燃烧更旺,发白光,放出热量,瓶壁有水雾,生成能使澄清石灰水变浑浊的无色气体有关的知识:(1)氧气是一种化学性质比较活泼的气体,在一定的条件下,能与许多物质发生反应。在这些反应中,氧气提供氧,称为氧化反应。氧气便是常见的氧化剂;(2)物质在纯氧气中燃烧程度比空气中燃烧要剧烈。说明物质燃烧程度,与氧气的浓度大小成正比;(3)物质燃烧时有的有火焰,有的会发光,有的会冒烟。一般来说,气体燃烧会有火焰产生,固体直接燃烧,产生光或者火星。生成物有固体,一般都会产生烟,即固体小颗粒;(4)物质与氧气反应不一定是燃烧现象,如缓慢氧化。[教师讲解]物质与氧气所发生的反应属于氧化反应。氧化反应可分为剧烈氧化(通常情况下的燃烧)和缓慢氧化(举几例说明)。讨论:剧烈氧化和缓慢氧化的相同点与不同点相同点:____________________________________________________不同点:____________________________________________________[师生总结]氧气是一种化学性质比较活泼的气体,能与许多物质发生氧化反应。[学生阅读]课本氧气的用途。...