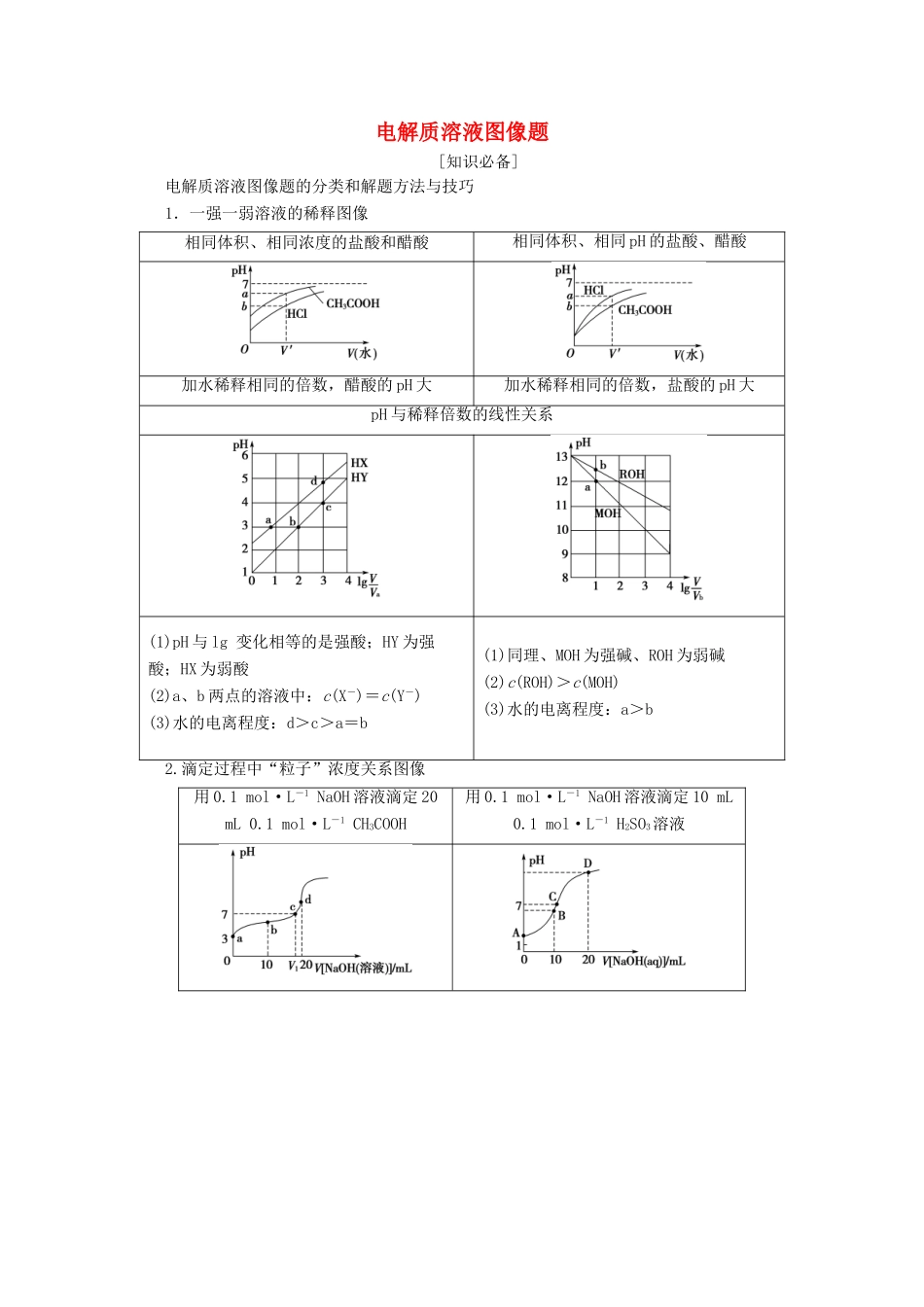
电解质溶液图像题[知识必备]电解质溶液图像题的分类和解题方法与技巧1.一强一弱溶液的稀释图像相同体积、相同浓度的盐酸和醋酸相同体积、相同pH的盐酸、醋酸加水稀释相同的倍数,醋酸的pH大加水稀释相同的倍数,盐酸的pH大pH与稀释倍数的线性关系(1)pH与lg变化相等的是强酸;HY为强酸;HX为弱酸(2)a、b两点的溶液中:c(X-)=c(Y-)(3)水的电离程度:d>c>a=b(1)同理、MOH为强碱、ROH为弱碱(2)c(ROH)>c(MOH)(3)水的电离程度:a>b2
滴定过程中“粒子”浓度关系图像用0
1mol·L-1NaOH溶液滴定20mL0
1mol·L-1CH3COOH用0
1mol·L-1NaOH溶液滴定10mL0
1mol·L-1H2SO3溶液(1)巧妙抓住“一半”“恰好”“中性”“过量”“二倍”点,突破“粒子”浓度关系(2)抓住“关键点”中以下问题:①参加反应溶质量的关系②溶质的成分③溶质中各成分量的关系④溶液的酸碱性等(3)正确使用电荷守恒和物料守恒解决问题3
分布系数与pH关系曲线图像一元弱酸(以CH3COOH为例)二元酸(以草酸H2C2O4为例)δ0为CH3COOH分布系数,δ1为CH3COO-分布系数δ0为H2C2O4分布系数、δ1为HC2O分布系数、δ2为C2O分布系数利用曲线的交点确定弱电解质每步的电离常数K1、K2、K3…根据图像确定不同pH点微粒间的关系4
对数——pH曲线图像题H2Y与NaOH溶液的反应H2X与NaOH溶液的反应(1)识图像:观察横坐标、纵坐标含义,找到横坐标的零点,即lg=0和lg=0的点
(2)找联系:二元弱酸H2X分步电离,H2XH++HX-,HX-H++X2-,第一步电离要远远大于第二步的电离,即K1>K2、c(H+)1>c(H+)2
(3)思原理:涉及到电离平衡常数,写出K1(H2X)=,K2(H2X)=