第4课时分子空间构型与分子性质[课型标签:知识课基础课]知识点一分子空间构型1
杂化轨道理论(1)杂化轨道概念:在外界条件的影响下,原子内部能量相近的原子轨道重新组合的过程叫原子轨道的杂化,组合后形成的一组新的原子轨道,叫杂化原子轨道,简称杂化轨道
(2)杂化轨道的类型与分子空间构型的关系2
价电子对互斥理论(1)理论要点①价电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低
②孤对电子的排斥力较大,孤对电子越多,排斥力越强,键角越小
(2)判断分子或离子空间构型“三步曲”第一步:确定中心原子上的价电子对数a为中心原子的价电子数,b为与中心原子结合的原子最多能接受的电子数,x为与中心原子结合的原子数
如NH3的中心原子为N,a=5,b=1,x=3,所以中心原子孤电子对数=(a-xb)=×(5-3×1)=1
第二步:确定价电子对的空间构型由于价电子对之间的相互排斥作用,它们趋向于尽可能的相互远离,这样已知价电子对的数目,就可以确定它们的空间构型
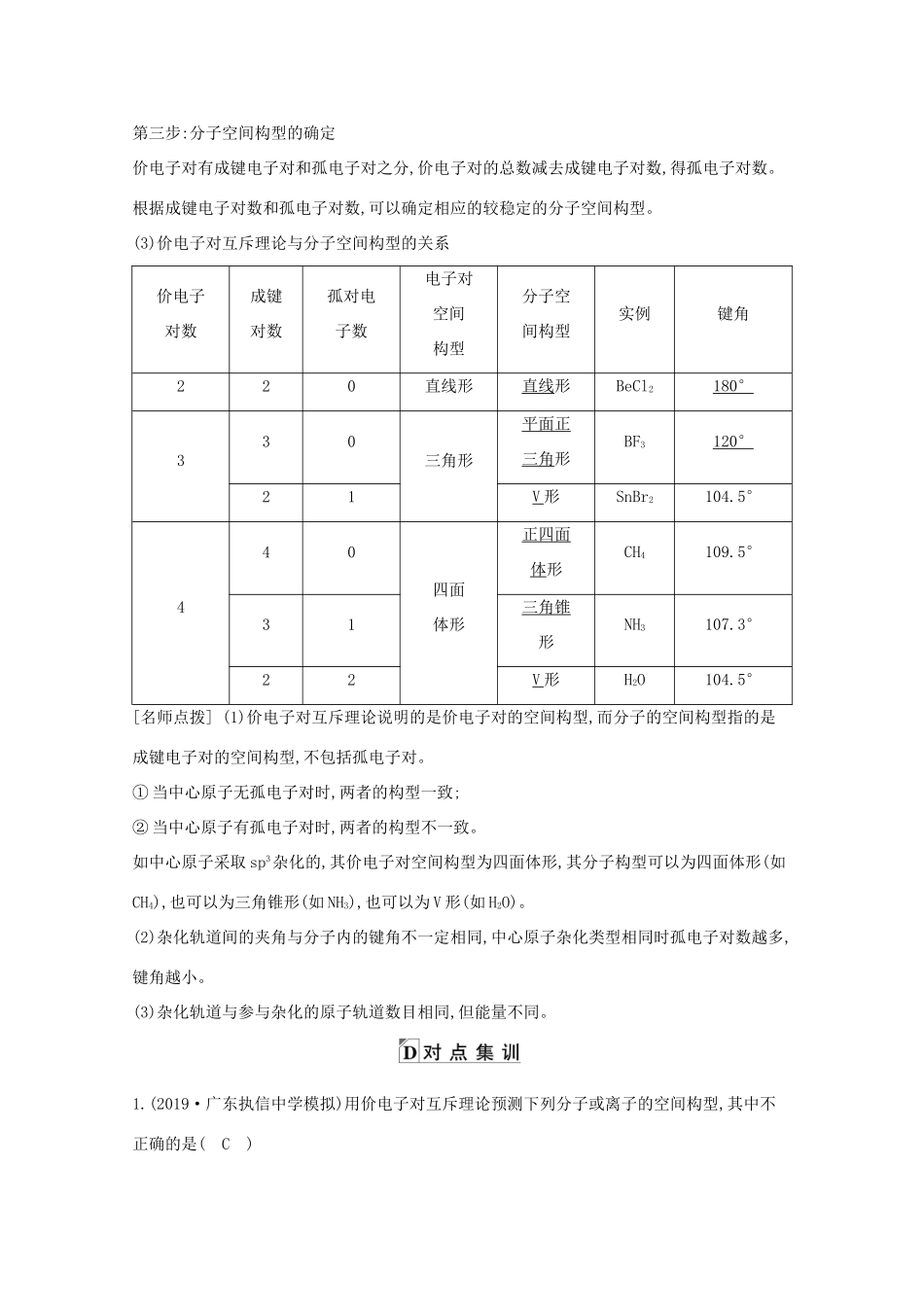
第三步:分子空间构型的确定价电子对有成键电子对和孤电子对之分,价电子对的总数减去成键电子对数,得孤电子对数
根据成键电子对数和孤电子对数,可以确定相应的较稳定的分子空间构型
(3)价电子对互斥理论与分子空间构型的关系价电子对数成键对数孤对电子数电子对空间构型分子空间构型实例键角220直线形直线形BeCl2180°330三角形平面正三角形BF3120°21V形SnBr2104
5°440四面体形正四面体形CH4109
5°31三角锥形NH3107
3°22V形H2O104
5°[名师点拨](1)价电子对互斥理论说明的是价电子对的空间构型,而分子的空间构型指的是成键电子对的空间构型,不包括孤电子对
①当中心原子无孤电子对时,两者的构型一致;②当中心原子有孤电子对时,两者的构型不一致
如中心原子采取sp3杂化的,其价电子对空间构型为四