第1页共8页编号:时间:2021年x月x日书山有路勤为径,学海无涯苦作舟页码:第1页共8页国家医疗器械质量公告[(2006)第6期,总第29期]国家食品药品监督管理局发布2006年6月为加强对医疗器械的监督管理,规范市场秩序,保障医疗器械产品使用安全、有效,2005年,国家食品药品监督管理局组织对角膜接触镜、外科缝线及缝合针、牙科藻酸盐印模材料进行了产品质量监督抽验
现将结果予以公告
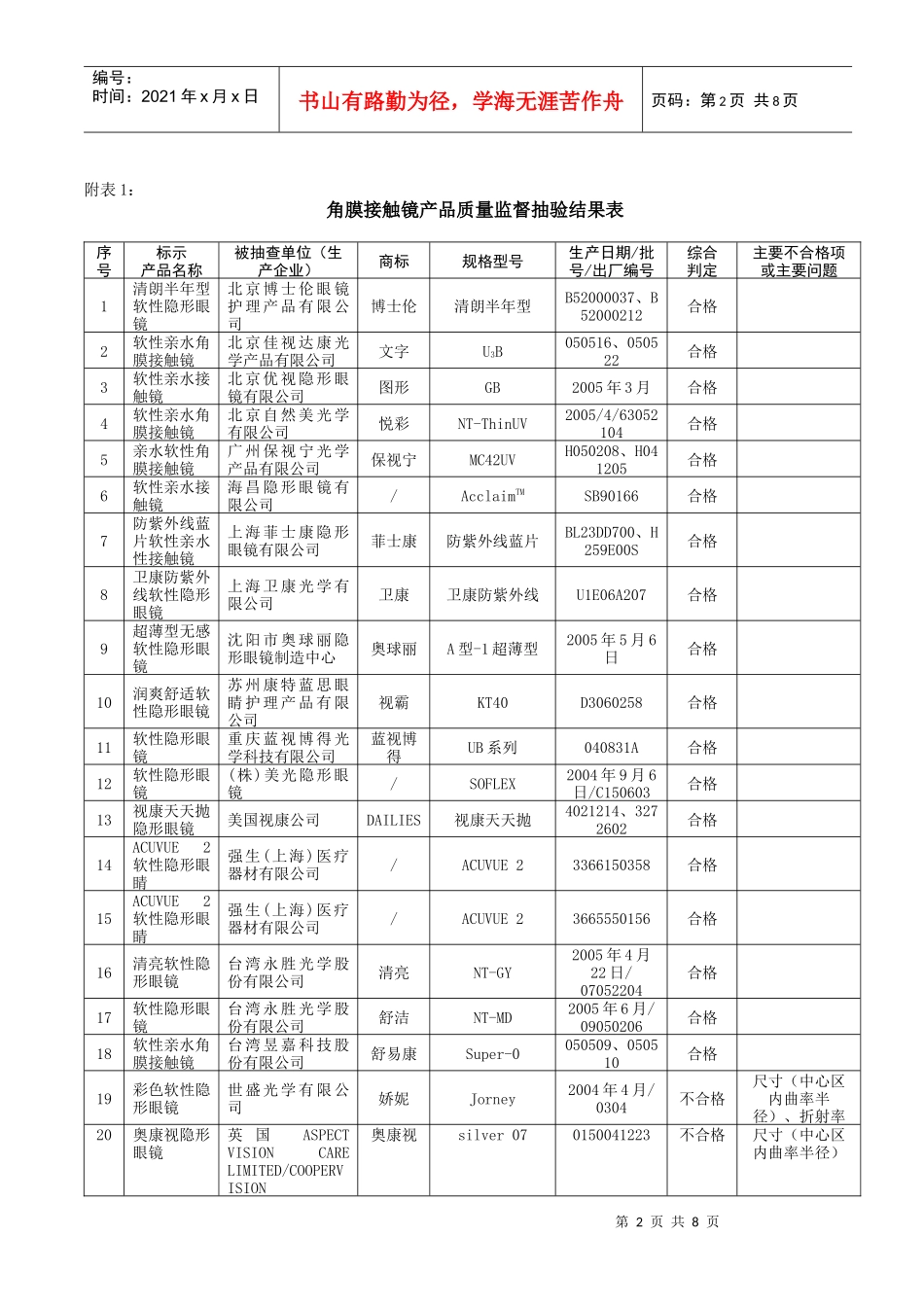
一、角膜接触镜此次抽验北京、辽宁、上海、江苏、广东、重庆、陕西等7个省(市)11家生产企业和8家经营单位的20批产品,涉及18家标示生产企业
依据国家标准GB11417
2—89《软性亲水接触镜》及1997年标准修改单、注册产品标准、ISO10344:1996《光学和光学仪器接触镜测试用盐溶液》、ISO8599:1994《光学和光学仪器接触镜光谱和透光率的测定》、ISO9337-1:1999《接触镜后顶点焦度测定第一部分使用手调聚焦式焦度测试方法》、ISO9338:1996《光学和光学仪器接触镜直径的测定》、ISO9913-1:1996《光学和光学仪器接触镜FATT法测定透氧系数与透氧量》、ISO9914:1995《光学和光学仪器接触镜材料折射率测定》、GB/T14233
1《医用输液、输血、注射器具检验方法》、GB/T14437-93《产品质量计数一次监督抽样检验程序》、ISO10338:1996《光学和光学仪器接触镜曲率半径的测定》进行检验
检验项目为:顶焦度、尺寸(中心区内曲率半径、总直径)、杂质和表面缺陷、透氧系数、折射率、透过率、灭菌等7项指标
经检验,18批产品被检验项目合格,2批产品被检验项目不合格(见附表1)
不合格产品的主要问题是尺寸(中心区内曲率半径)、折射率等指标不符合标准规定
二、外科缝线及缝合针此次抽验全国31个省(区、市)23家生产企业和65家经营使用单位的116批