专题限时集训(三)突破点5[建议用时:45分钟]1.(2016·临沂质检)下列关于元素周期表的说法中正确的是()A.同一主族元素的原子序数的差不可能为10B.同周期第ⅡA族与第ⅢA族元素的原子序数差值一定为1C.催化剂一般在金属元素与非金属元素的分界线处寻找D.过渡元素全部是金属元素D[第ⅠA族的H和Na的原子序数相差10,A项错误;从第四周期开始,同周期第ⅡA族与第ⅢA族元素的原子序数差值不为1,B项错误;催化剂应在过渡元素区域寻找,C项错误
]2.(2016·江西10月联考)某同学设计如图元素周期表,已知Z元素的最外层电子数是次外层的3倍
空格中均有对应的元素填充,以下说法正确的是()A.白格中都是主族元素,灰格中都是副族元素B.X和Z形成的化合物只有两种C.X、Y元素最高价氧化物对应水化物的酸性:X>YD.X、Y、Z的气态氢化物中最稳定的是X的氢化物C[白格中都是主族元素,灰格中是副族元素和Ⅷ族元素,A项错误;X为N,Z为O,二者形成的化合物有N2O、NO、N2O3、NO2、N2O4、N2O5等,B项错误;X为N,Y为P,非金属性:N>P,故最高价氧化物对应水化物的酸性:HNO3>H3PO4,C项正确;X为N、Y为P、Z为O,Z的非金属性最强,故Z的氢化物稳定性最强,D项错误
]3.(2016·河南商丘二模)在元素周期表短周期元素中,X元素与Y、Z、W三种元素相邻
X、Y的原子序数之和等于Z的原子序数,这四种元素原子的最外层电子数之和为20
下列判断一定正确的是()【导学号:14942025】A.单质熔点:Z>WB.离子半径:XZC[根据题中条件可知X、Y、Z、W依次为氮、氧、磷、碳
金刚石的熔点高于磷单质,A项错误;X、Y在同周期,且Y的核电荷数较大,离子半径:YZ,D错误
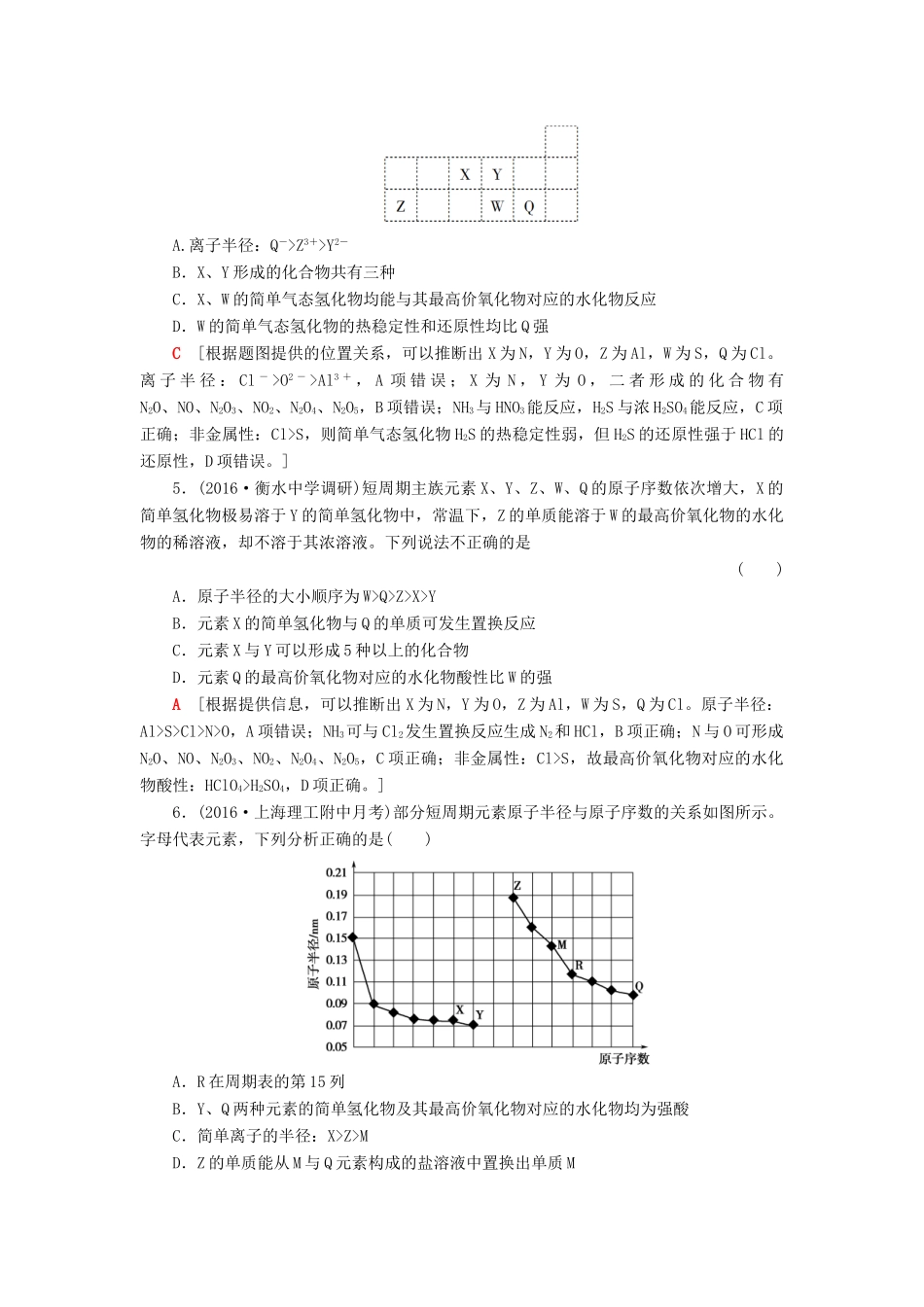
]4.元素周期表中短周期的一部分如图所示,下列关于X、Y、Z、W、Q的说法正确的是()A