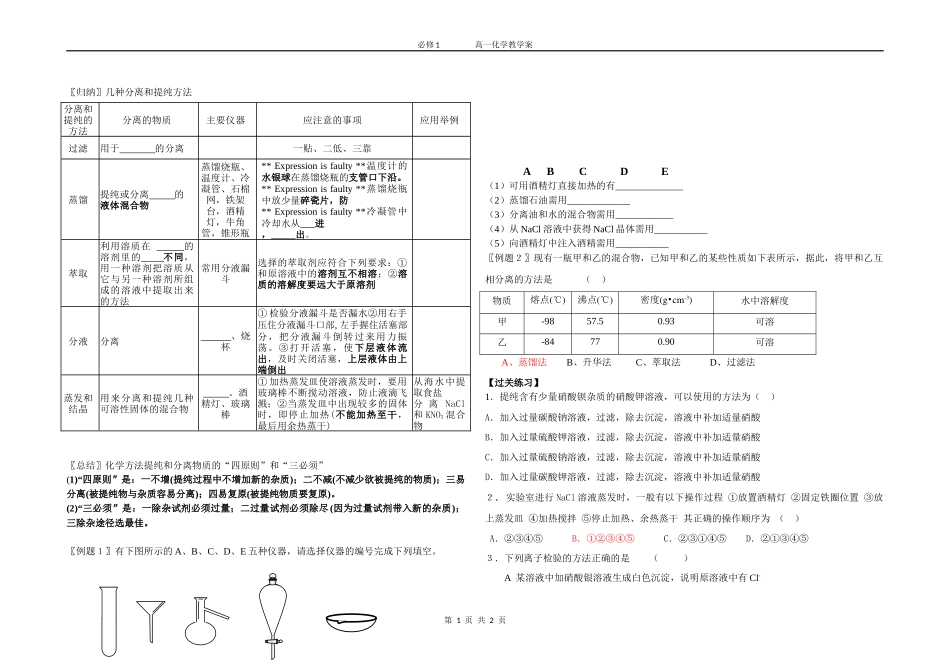
必修1高一化学教学案〖归纳〗几种分离和提纯方法〖总结〗化学方法提纯和分离物质的“四原则”和“三必须”(1)“四原则”是:一不增(提纯过程中不增加新的杂质);二不减(不减少欲被提纯的物质);三易分离(被提纯物与杂质容易分离);四易复原(被提纯物质要复原)。(2)“三必须”是:一除杂试剂必须过量;二过量试剂必须除尽(因为过量试剂带入新的杂质);三除杂途径选最佳。〖例题1〗有下图所示的A、B、C、D、E五种仪器,请选择仪器的编号完成下列填空。ABCDE(1)可用酒精灯直接加热的有______________(2)蒸馏石油需用_____________(3)分离油和水的混合物需用____________(4)从NaCl溶液中获得NaCl晶体需用___________(5)向酒精灯中注入酒精需用___________〖例题2〗现有一瓶甲和乙的混合物,已知甲和乙的某些性质如下表所示,据此,将甲和乙互相分离的方法是()物质熔点(℃)沸点(℃)密度(g•cm-3)水中溶解度甲-9857.50.93可溶乙-84770.90可溶A、蒸馏法B、升华法C、萃取法D、过滤法【过关练习】1.提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为()A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸2.实验室进行NaCl溶液蒸发时,一般有以下操作过程①放置酒精灯②固定铁圈位置③放上蒸发皿④加热搅拌⑤停止加热、余热蒸干其正确的操作顺序为()A.②③④⑤B.①②③④⑤C.②③①④⑤D.②①③④⑤3.下列离子检验的方法正确的是()A某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl-第1页共2页分离和提纯的方法分离的物质主要仪器应注意的事项应用举例过滤用于的分离一贴、二低、三靠蒸馏提纯或分离的液体混合物蒸馏烧瓶、温度计、冷凝管、石棉网,铁架台,酒精灯,牛角管,锥形瓶**Expressionisfaulty**温度计的水银球在蒸馏烧瓶的支管口下沿。**Expressionisfaulty**蒸馏烧瓶中放少量碎瓷片,防**Expressionisfaulty**冷凝管中冷却水从进,出。萃取利用溶质在的溶剂里的不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法常用分液漏斗选择的萃取剂应符合下列要求:①和原溶液中的溶剂互不相溶;②溶质的溶解度要远大于原溶剂分液分离、烧杯①检验分液漏斗是否漏水②用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来用力振荡。③打开活塞,使下层液体流出,及时关闭活塞,上层液体由上端倒出蒸发和结晶用来分离和提纯几种可溶性固体的混合物、酒精灯、玻璃棒①加热蒸发皿使溶液蒸发时,要用玻璃棒不断搅动溶液,防止液滴飞溅;②当蒸发皿中出现较多的固体时,即停止加热(不能加热至干,最后用余热蒸干)从海水中提取食盐分离NaCl和KNO3混合物必修1高一化学教学案B某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中有SO42-C某溶液中加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+D某溶液加稀硫酸生成白色沉淀,说明原溶液中有CO32-4.某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中()A.一定有SO42-B.可能有SO42-或Ag+C.一定无Ag+D.还可能有CO32-5.下列各组物质的分离可用分液漏斗的是()A、乙醇和水B、苯和食盐水C、黄河水中的泥沙与水D、食盐水中获得食盐6.下列混合物的分离方法不可行的是()A、互溶的液体混合物可用分液方法分离B、互不相溶的液态混合物可用分液方法分离C、沸点不同的液体混合物可用蒸馏方法分离D、溶于水的固体与难溶于水的固体形成的混合物可用溶解、过滤、蒸发的方法分离7.(08年扬州市学业模拟)下列实验操作中错误的是A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出D.萃取操作时,应选择有机萃取剂,如:苯、四氯化碳等9.如图所示,①、②、③、④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容...