2014届三厂中学高三化学一轮复习讲义基本理论编制:张键审核:陈达2013-11-08总编号:371专题十二水溶液中的离子平衡第四、五课时盐类水解【课堂目标】(第四课时)1
会书写水解离子方程式2
能运用盐类水解的规律判断常见盐溶液的酸碱性3
了解盐类水解的原理,能说明影响盐类水解程度的主要因素【基础梳理】活动一:盐类水解的原理(1)水解离子方程式的书写①NH4+:
②CH3COO-:
③Al3+:
④CO32-:
(2)TiCl4水解的化学方程式:
注意点:辨析:()①lL0
5mol/LNa2CO3溶液中含有CO32-数为0
5NA()②1mol•L-1的FeCl3溶液中含有的Fe3+数目小于1NA()③纯碱溶液呈碱性的原理:CO32-+2H2OH2CO3+2OH-()④向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体()⑤pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同活动二:影响盐类水解程度的因素1
内因(1)比较相同物质的量浓度下列物质的酸碱性强弱①H2CO3、CH3COOH、C6H5OH(苯酚)、H2CO3-酸性:>>>
②Na2CO3、NaHCO3、CH3COONa、C6H5ONa(苯酚钠)碱性:>>>
(2)结论:相同条件下,酸的酸性越弱,其对应的弱酸根离子水解程度越,溶液的碱性越
——越弱越水解
(3)辨析:()测定相同物质的量浓度Na2SO4、Na2CO3溶液的pH,pH:Na2SO4<Na2CO3结论:酸性H2SO4>H2CO3,非金属性S>C2014届三厂中学高三化学一轮复习讲义基本理论编制:张键审核:陈达2013-11-08总编号:3722
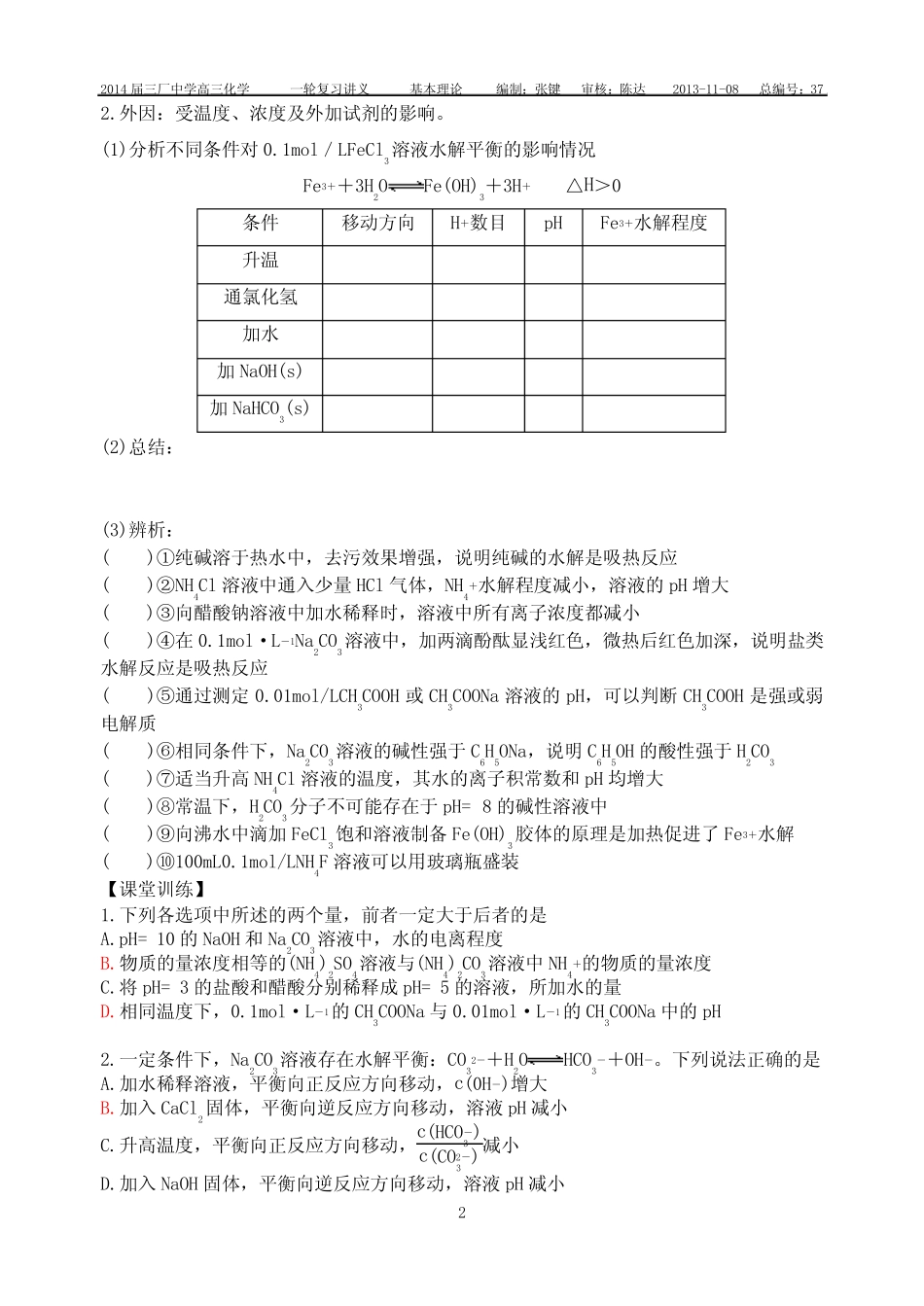
外因:受温度、浓度及外加试剂的影响
(1)分析不同条件对0
1mol/LFeCl3溶液水解平衡的影响情况Fe3++3H2OFe(OH)3+3H+△H>0条件移动方向H+数目