原电池和电解池1.原电池和电解池的比较:装置实例使氧化还原反应中电子作定向移动,从而形成电流
这种把化学能转变为电能的装置叫原理做原电池
形成条件反应类自发的氧化还原反应型由电极本身性质决定:电极名正极:材料性质较不活泼的电极;称负极:材料性质较活泼的电极
电极反应电子流负极→正极向电流方正极→负极向能量转化学能→电能化①抗金属的电化腐蚀;应用②实用电池
2.化学腐蚀和电化腐蚀的区别化学腐蚀电化腐蚀③电冶(冶炼Na、Mg、Al);④精炼(精铜)
①电解食盐水(氯碱工业);②电镀(镀铜);电能→化学能电源正极→阳极;阴极→电源负极电源负极→阴极;阳极→电源正极负极:Zn-2e-=Zn2+(氧化反应)正极:2H++2e-=H2↑(还原反应)阴极:连电源的负极;阴极:Cu2++2e-=Cu(还原反应)阳极:2Cl--2e-=Cl2↑(氧化反应)阳极:连电源的正极;由外电源决定:非自发的氧化还原反应①电极:两种不同的导体相连;②电解质溶液:能与电极反应
为化学能的装置叫做电解池
①电源;②电极(惰性或非惰性);③电解质(水溶液或熔化态)
化还原反应的过程叫做电解
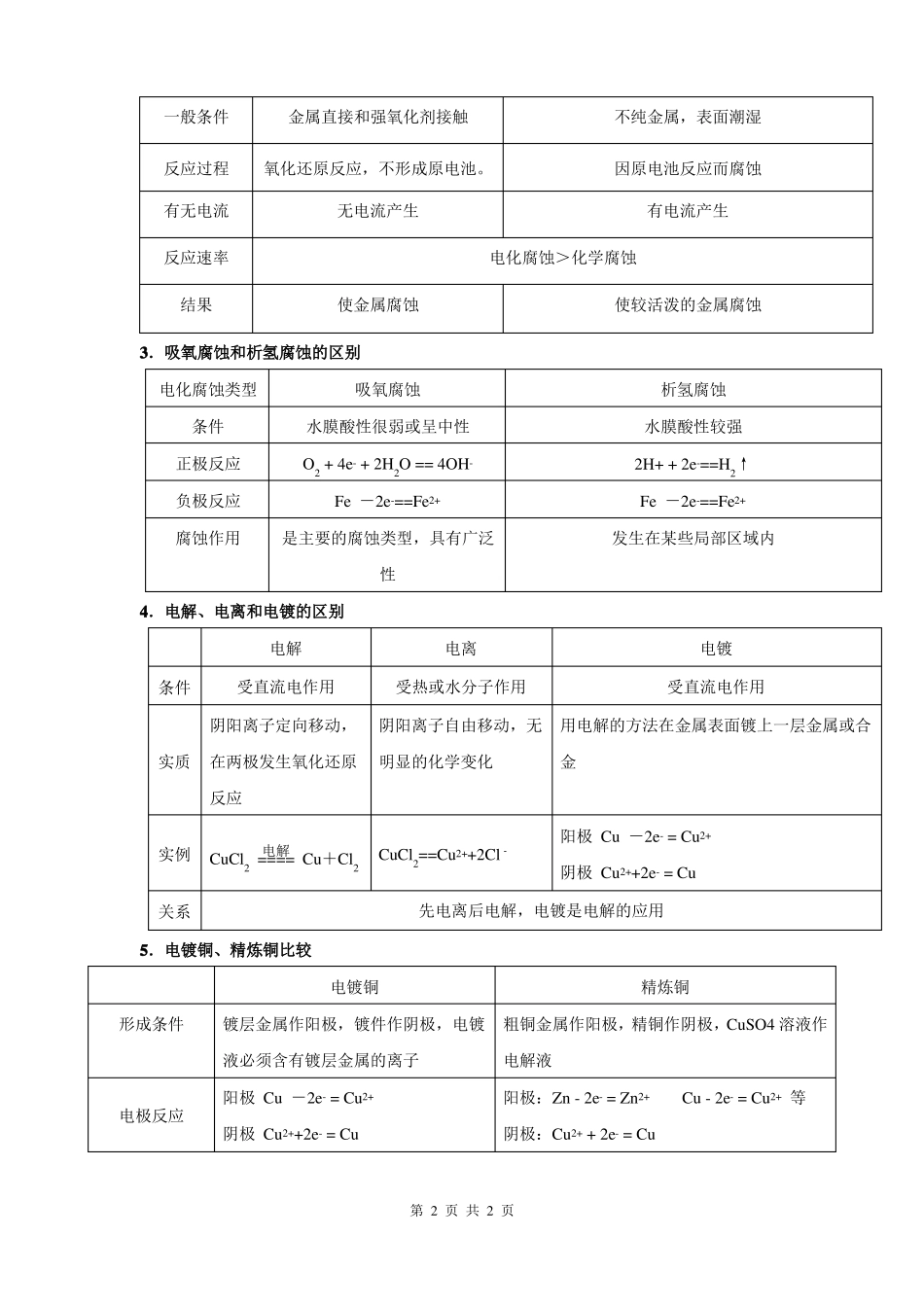
这种把电能转变使电流通过电解质溶液而在阴、阳两极引起氧原电池电解池第1页共1页一般条件反应过程有无电流反应速率结果金属直接和强氧化剂接触氧化还原反应,不形成原电池
无电流产生不纯金属,表面潮湿因原电池反应而腐蚀有电流产生电化腐蚀>化学腐蚀使金属腐蚀使较活泼的金属腐蚀3.吸氧腐蚀和析氢腐蚀的区别电化腐蚀类型条件正极反应负极反应腐蚀作用吸氧腐蚀水膜酸性很弱或呈中性O2+4e-+2H2O==4OH-Fe-2e-==Fe2+是主要的腐蚀类型,具有广泛性4.电解、电离和电镀的区别条件电解受直流电作用阴阳离子定向移动,实质在两极发生氧化还原反应2+电解实例CuCl2====Cu+Cl2CuCl2==Cu+2Clˉ析氢腐蚀水膜酸性较强2