第五章物质结构元素周期律学案三、化学键与分子结构2008
10●教学点睛本部分包括高中化学教材第一册中的第五章第四自然节和第二册第一章第二节和第三册第一单元第一自然节等内容
主要考点有:①离子键、共价键的形成及特征;②用电子式表示离子化合物、共价化合物的形成;③极性键、非极性键、极性分子与非极性分子的概念;④极性分子、非极性分子的判断;⑤分子间作用力
复习本部分内容时应注意以下几点:(1)搞清化学键的概念,引导学生分析由于形成“稳定结构”,而导致元素的原子形成不同类型的化学键
常见的类型主要有离子键和共价键,列表进行比较
重点是让学生善于判断化合物中原子之间以何种键相结合,并能用电子式正确表示离子化合物和共价化合物的形成过程及化合物的结构
(2)引导学生写出常见物质(如N2、HCl、H2O、CO2、NH3等)的电子式和结构式,指出化学键类型,判断分子有无极性
在此基础上归纳总结分子的极性与共价键的极性之间的关系,判断分子极性的方法规律等
(3)在复习过程中,可启发学生分析思考下列问题:①卤素单质I2的熔点比Br2的熔点高,原因是什么
②为什么碘在四氯化碳中的溶解度比在水中的溶解度大
③为什么水的熔沸点比硫化氢的熔沸点高得多
归纳总结有关知识规律,强化知识的理解应用
(4)本部分内容复习可安排一课时
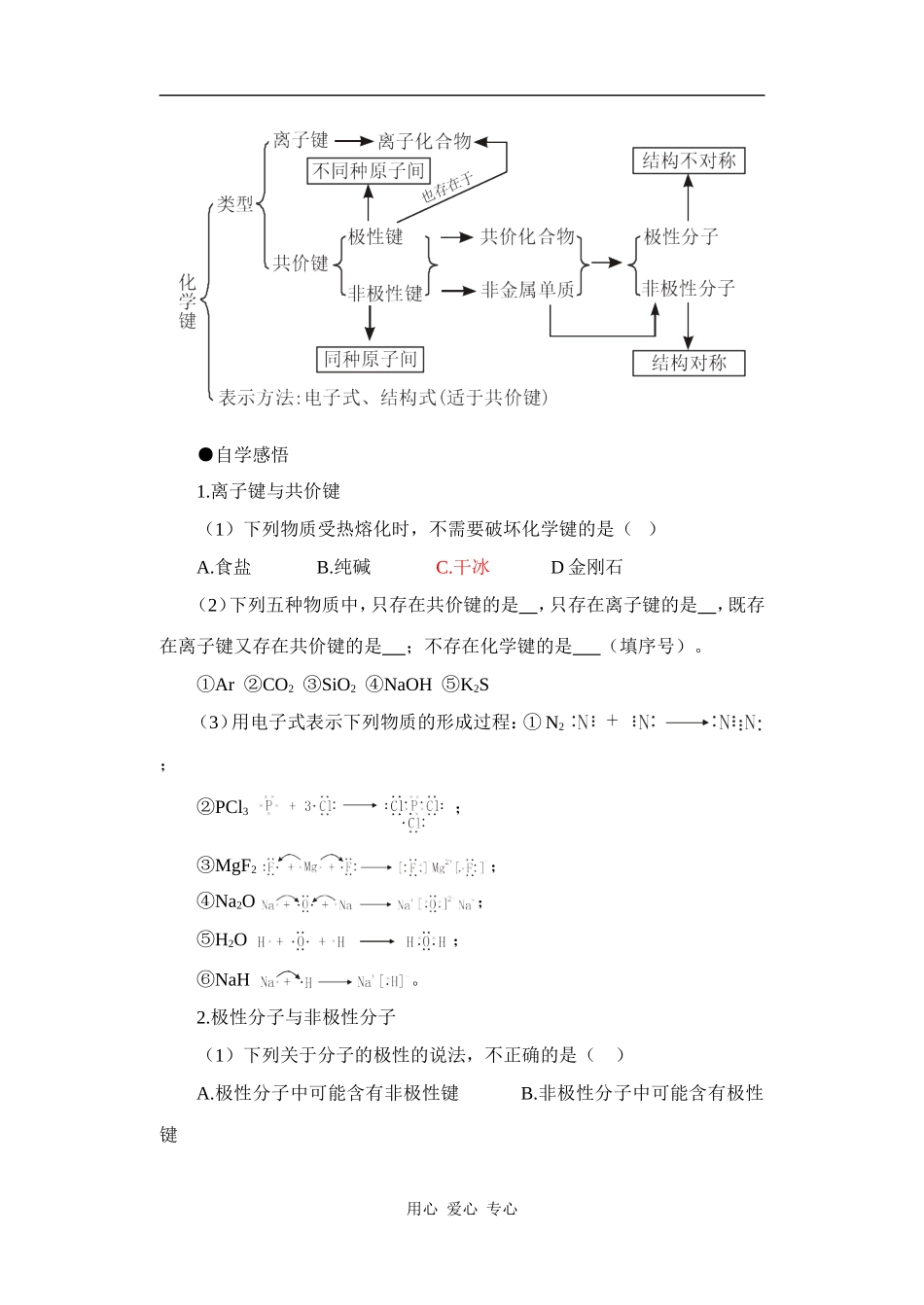
知识梳理●网络构建用心爱心专心●自学感悟1
离子键与共价键(1)下列物质受热熔化时,不需要破坏化学键的是()A
干冰D金刚石(2)下列五种物质中,只存在共价键的是,只存在离子键的是,既存在离子键又存在共价键的是;不存在化学键的是(填序号)
①Ar②CO2③SiO2④NaOH⑤K2S(3)用电子式表示下列物质的形成过程:①N2;②PCl3;③MgF2;④Na2O;⑤H2O;⑥NaH
极性分子与非极性分子(1)下列关于分子的极性的说法,不正确的是()A