蛋白质的错误折叠郑晓惠10281034生物物理学系主要内容:1蛋白质的正常折叠及保护机制2蛋白质错误折叠与神经系统相关疾病3蛋白质错误折叠的机制4蛋白质错误折叠的致病机理5针对蛋白质错误折叠可采取的治疗途径6结语一蛋白质的正常折叠及保护机制根据分子生物学中心法则,生物遗传信息的传递是由DNA到RNA(转录)、RNA到蛋白质多肽链(翻译)、再由多肽链形成具有生物活性的蛋白质(折叠)进行的
目前对前两个过程已有相当深入和清晰的了解,但对后者尚不十分清楚
可以说蛋白质折叠是生物学中心法则中至今尚未解决的一个重大生物学问题
蛋白质是生物体内一切功能的执行者
具有完整一级结构的多肽链只有当其折叠形成正确的三维空间结构才能具有正常的生物学功能
如果这种折叠过程在体内发生故障,形成错误的空间结构,不但将丧失其生物学功能,甚至会引起疾病
在细胞内大多数天然蛋白质能自发的形成比较稳定的天然结构,或被配体和代谢因子所稳定
但约10-20%新合成的多肽链需要分子伴侣的帮助才能正常折叠
另外,约有20%新合成的多肽链不能形成正确的三维结构而被蛋白酶降解,包括由于错误转录和翻译形成的不完全蛋白质,翻译后受到化学损伤或其他因素引起的失活、去折叠或折叠错误的蛋白质
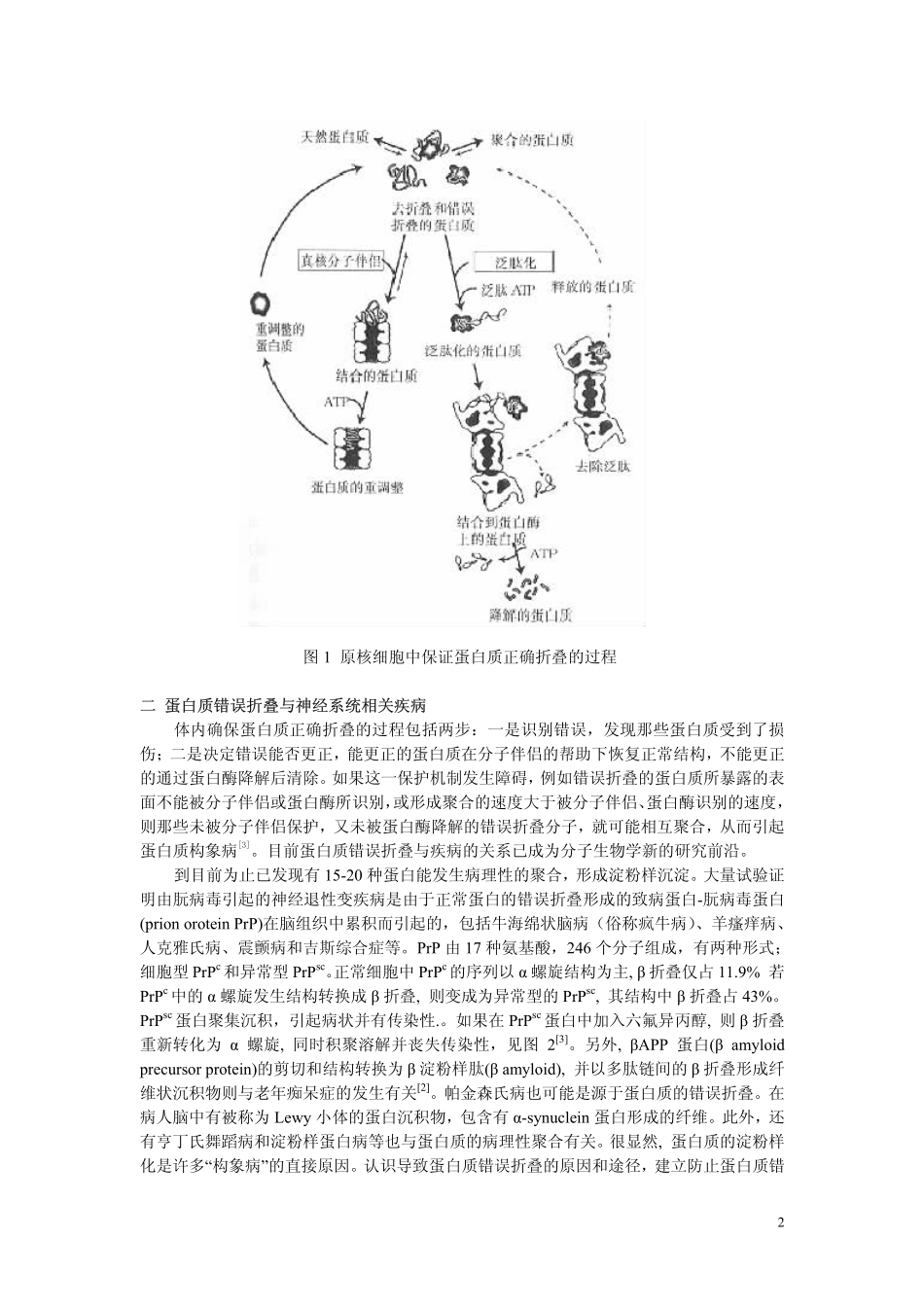
在真核细胞中,多余的蛋白质主要通过泛肽化(ubiquittination)过程降解,见图1[3]
分子伴侣实际上是生物克服细胞内大分子拥挤环境对蛋白质生物合成影响的进化产物
分子伴侣的共同特征是参与催化、介导其他多肽链或寡聚体蛋白质分子的折叠与组装,但不是蛋白质最终结构的一部分
它与靶蛋白的结合不具高度专一性,同一伴侣分子可促进多种氨基酸序列不同的多肽链折叠
它只是分子折叠的协助者,本身并不含正确折叠所必须的构象信息,而是通过阻止非天然多肽内部或相互间的不正确作用而发挥效能
至今为止发现的大多数分子伴侣属热休克蛋白的范畴
小分子伴侣,如热休克