一.气体状态参量温度T:宏观上表示物体的冷热程度;微观上标志分子的平均动能.体积V:宏观上气体体积等于容纳气体容器的容积;微观上与单位体积分子数关联.压强p:宏观上表示器壁在单位面积上受到的压力;微观上是由大量分子频繁撞击器壁产生的.§12-9气体压强和温度、体积间的关系温标:表示温度数值的方法;摄氏温标t:一标准大气压下,冰水混合温度为0℃;沸水温度为100℃;0~100的1/100为1℃热力学温标T:T=t+273
15K理想气体:分子间作用力可忽略,没有分子势能,内能为所有分子平均动能的总和
实际气体的温度越高、压强越小,越接近理想气体
常温、常压下的气体都可视为理想气体
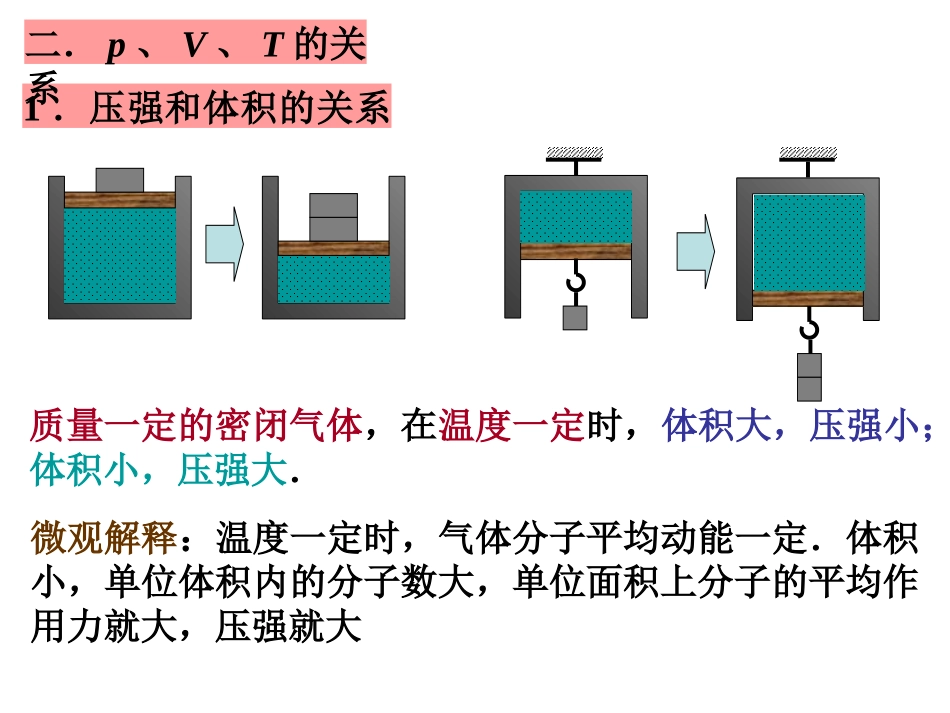
气体质量一定时,若气体处于一个稳定状态,则P、V、T三个参量不变;当气体状态发生变化,则P、V、T三个参量中有两个或三个参量发生变化1.压强和体积的关系微观解释:温度一定时,气体分子平均动能一定.体积小,单位体积内的分子数大,单位面积上分子的平均作用力就大,压强就大质量一定的密闭气体,在温度一定时,体积大,压强小;体积小,压强大.二.p、V、T的关系质量一定的密闭气体,在体积一定时,温度高,压强大;温度低,压强小2.压强和温度的关系微观解释:体积一定时,单位体积内的分子数一定.温度高,气体分子平均动能大,单位时间单位面积上撞击的分子多,撞击的平均作用力大,压强就大3.体积和温度的关系质量一定的密闭气体,在压强一定时,温度高,体积强大;温度低,体积小微观解释:压强一定时,单位体积内的分子数与分子平均动能的乘积一定.温度高,气体分子平均动能大,分子撞击的作用力大,撞击频繁;要保持压强一定,则要减小分子数密度,而分子总数不变,故必须增大体积一定质量的理想气体,温度越高、体积越小,则气体压强越大;温度越低、体积越大,则气体压强越小4.理想气体状态方程:vmvnP2)61(VTpkEnPCTpVR