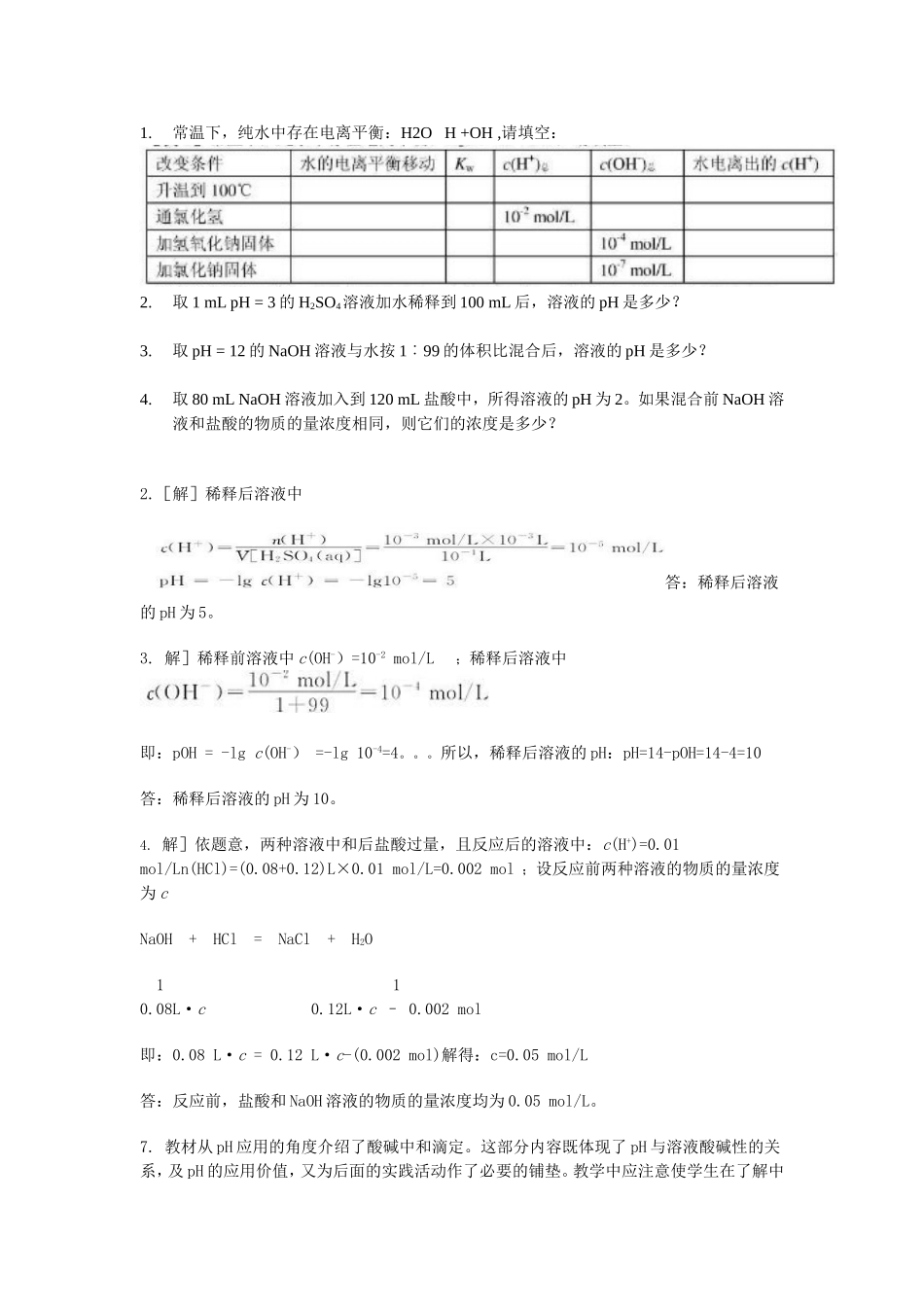
常温下,纯水中存在电离平衡:H2OH+OH,请填空:2
取1mLpH=3的H2SO4溶液加水稀释到100mL后,溶液的pH是多少
取pH=12的NaOH溶液与水按1︰99的体积比混合后,溶液的pH是多少
取80mLNaOH溶液加入到120mL盐酸中,所得溶液的pH为2
如果混合前NaOH溶液和盐酸的物质的量浓度相同,则它们的浓度是多少
[解]稀释后溶液中答:稀释后溶液的pH为5
解]稀释前溶液中c(OH-)=10-2mol/L;稀释后溶液中即:pOH=-lgc(OH-)=-lg10-4=4
所以,稀释后溶液的pH:pH=14-pOH=14-4=10答:稀释后溶液的pH为10
解]依题意,两种溶液中和后盐酸过量,且反应后的溶液中:c(H+)=0
01mol/Ln(HCl)=(0
12)L×0
01mol/L=0
002mol;设反应前两种溶液的物质的量浓度为cNaOH+HCl=NaCl+H2O110
08L·c0
12L·c–0
002mol即:0
08L·c=0
12L·c-(0
002mol)解得:c=0
05mol/L答:反应前,盐酸和NaOH溶液的物质的量浓度均为0
05mol/L
教材从pH应用的角度介绍了酸碱中和滴定
这部分内容既体现了pH与溶液酸碱性的关系,及pH的应用价值,又为后面的实践活动作了必要的铺垫
教学中应注意使学生在了解中和滴定方法和原理的同时,体会pH在这种最常用的定量分析中的作用,以及酸碱反应过程中溶液酸碱性与pH的动态变化
1、实验表明,液态时,纯硫酸的导电性强于纯水
已知液态电解质都能像水那样自身电离而建立电离平衡,且在一定条件下都有各自的离子积常数
问在25℃时,纯硫酸的离子积常数K和水的离子积常数Kw关系为()A、K>KwB、K=KwC、K<KwD、无法比较2、纯水在25℃和80℃时的氢离子浓度,