1溶液)()BBmolbkg=溶质的物质的量(溶剂的质量Bmwm=溶质溶液=)()BBmolcL溶质的物质的量(混合物体积=BBnxn总[例3-1]23g乙醇溶于500g水中,此溶液的密度是0
992g·mL-1
计算:(1)乙醇的质量摩尔浓度b;(2)乙醇的体积摩尔浓度c(物质的量的浓度);(3)乙醇的质量分数;(4)乙醇的摩尔分数
第三章水溶液中酸碱平衡和沉淀平衡中国石油大学《《大学化学大学化学Ⅰ》Ⅰ》课件课件3
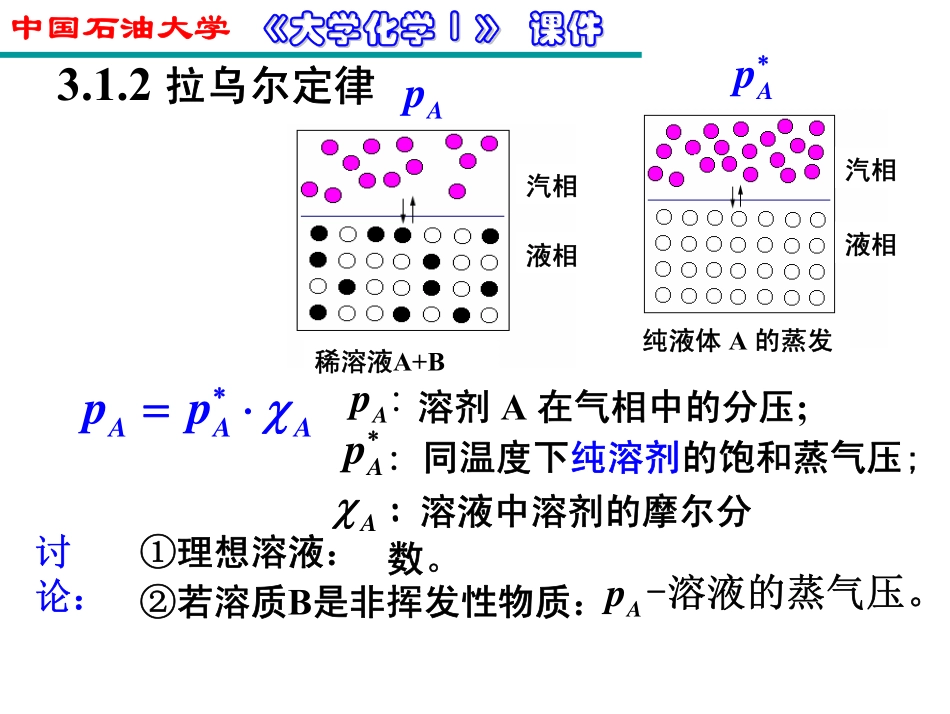
1溶液组成的表示方法∗=⋅AAAppχ:同温度下纯溶剂的饱和蒸气压;Ap∗Aχ:溶液中溶剂的摩尔分数
Ap:溶剂A在气相中的分压;3
2拉乌尔定律纯液体A的蒸发液相汽相∗Ap稀溶液A+B液相汽相Ap中国石油大学《《大学化学大学化学Ⅰ》Ⅰ》课件课件②若溶质B是非挥发性物质:①理想溶液:讨论:Ap-溶液的蒸气压
BBABnnnχ=+Δ=⋅*ABppχ*AApppΔ=−(/)BBAAAnnnmM≈=ABMb=⋅1、稀溶液蒸气压下降3
3稀溶液的依数性*AABBppMbKbΔ≈⋅⋅=⋅�难挥发的非电解质稀溶液,蒸气压下降值只取决于溶剂的本性及溶液的质量摩尔浓度
中国石油大学《《大学化学大学化学Ⅰ》Ⅰ》课件课件沸点升高值:2、稀溶液的沸点上升Kb=0
515K·kg-1·mol-1*bbbTTTΔ=−bbBTKbΔ=⋅Kb--溶剂的摩尔沸点上升常数
p16:表1
3一些溶剂的摩尔沸点上升常数思考:浓度同为0
01mol·kg-1的丙三醇的乙醇溶液和水溶液,它们的沸点升高值是否相同
中国石油大学《《大学化学大学化学Ⅰ》Ⅰ》课件课件3、稀溶液凝固点下降溶液凝固点降低值:Kf=1
853K·kg-1·mol-1*fffTTTΔ=−ffBTKbΔ=⋅Kf---溶剂摩尔凝固点下降常数
[例3-2]0
9g醋酸溶于50
0g水中,实验测得溶液的凝固点为272