第四节难溶电解质的溶解平衡第四节难溶电解质的溶解平衡第三章水溶液中的离子平衡•一、溶解平衡•1
不同的固体物质在水中的溶解度不同,有的很大,有的很小,但无论大小,都有一定的溶解度
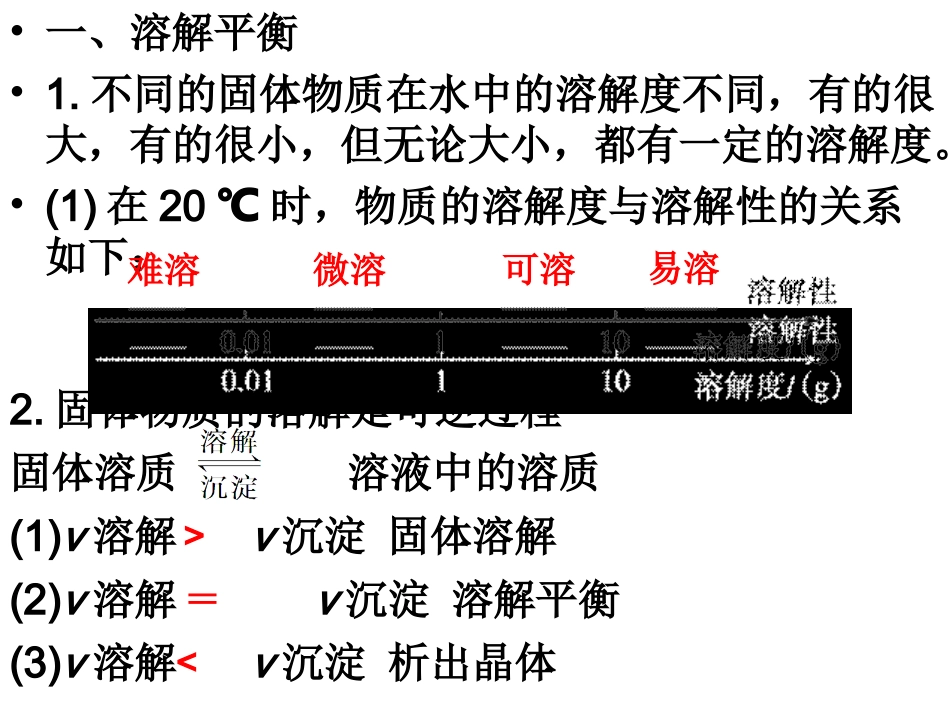
•(1)在20℃时,物质的溶解度与溶解性的关系如下:难溶微溶可溶易溶2
固体物质的溶解是可逆过程固体溶质溶液中的溶质(1)v溶解v沉淀固体溶解(2)v溶解v沉淀溶解平衡(3)v溶解v沉淀析出晶体>=>>2.写出下列沉淀溶解平衡的溶度积常数的表达式(1)AgCl(s)Ag+(aq)+Cl-(aq)(2)Fe(OH)3(s)Fe3+(aq)+3OH-(aq)(3)AmBn(s)mAn+(aq)+nBm-(aq)3
通过比较溶度积与离子积Qc的相对大小,可以判断难溶电解质在给定条件下平衡进行方向:(1)Qc>Ksp,溶液过饱和,有沉淀析出,直至溶液饱和,达到新的平衡
(2)Qc=Ksp,溶液饱和,沉淀与溶解处于平衡状
(3)QcKsp,c(Ba2+)=c(SO42-)C.c(Ba2+)·c(SO42-)=Ksp,c(Ba2+)>c(SO42-)D.c(Ba2+)·c(SO42-)≠Ksp,c(Ba2+)