第6讲离子共存与离子推断一、离子共存离子共存问题是离子反应条件和本质的最直接应用
所谓几种离子在同一溶液中能大量共存,就是指离子之间不发生反应;若离子之间能发生反应,则不能大量共存
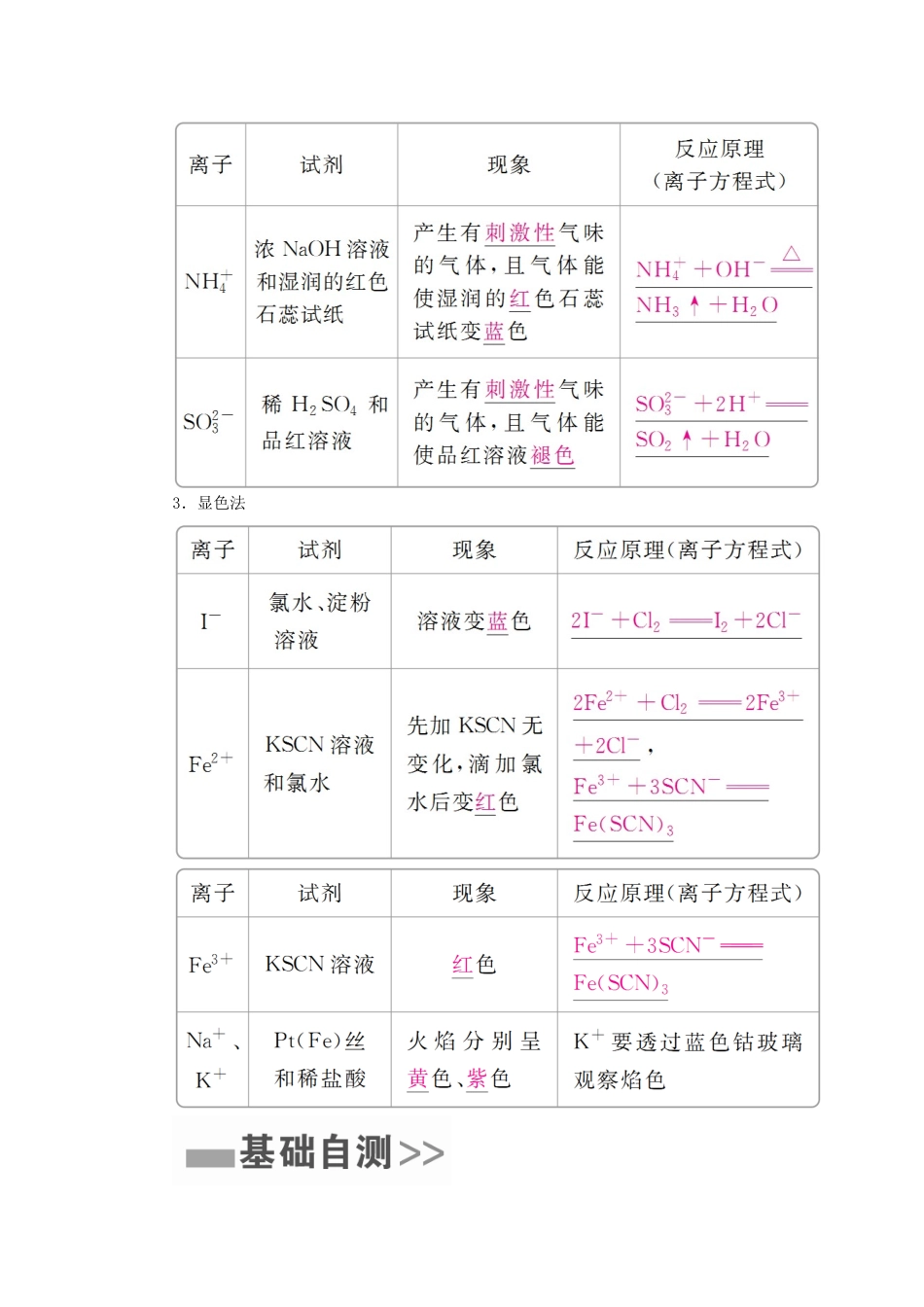
二、掌握离子检验的三种方法1.沉淀法2.气体法3.显色法1.正误判断,正确的画“√”,错误的画“×”
(1)向某溶液中加入BaCl2溶液,有白色沉淀生成,再加入稀盐酸,沉淀不消失,则溶液一定存在SO
()(2)向某溶液中加入Ba(NO3)2溶液,产生不溶于稀HNO3的白色沉淀,则溶液中一定存在SO
()(3)向某溶液中加入Ca(OH)2溶液,有白色沉淀生成,则溶液中一定存在CO
()(4)加入稀盐酸酸化的BaCl2溶液,出现白色沉淀,则溶液中可能有SO或Ag+
()(5)加入CaCl2溶液,有白色沉淀生成,溶液中一定存在CO
()(6)滴入硝酸酸化的BaCl2溶液,产生白色沉淀,溶液中一定存在SO
()答案(1)×(2)×(3)×(4)√(5)×(6)×2.教材改编题(据人教必修一P34T7)下列各组离子,在溶液中能大量共存的是()A.Na+、H+、Cl-、OH-B.K+、Mg2+、Cl-、SOC.Na+、OH-、NO、HCOD.K+、Cl-、H+、HCO答案B考点1离子共存典例1(2017·四川南充模拟)在指定条件下,下列各组离子一定不能大量共存的是()①能使红色石蕊试纸变蓝的溶液中:Na+、K+、CO、NO、AlO②c(H+)=0
1mol·L-1的溶液中:Cu2+、Al3+、SO、NO③能使碘化钾-淀粉试纸变蓝的溶液中:Na+、NH、S2-、Br-④由水电离出的c(H+)=10-12mol·L-1的溶液中:Na+、Mg2+、Cl-、HCO⑤加入铝粉能产生氢气的溶液中:NH、Fe2+、SO、NO⑥含有大量Fe3+的溶液中:NH、Na+、Cl-、SCN-A.①②③B.①③⑥C.③④⑤⑥D.②④