第26讲弱电解质的电离平衡目标要求1
从电离、离子反应、化学平衡的角度认识电解质水溶液的组成、性质和反应,如酸碱性、导电性等
认识弱电解质在水溶液中存在电离平衡,了解电离平衡常数的含义
能运用化学用语正确表示水溶液中的离子反应与平衡,能通过实验证明水溶液中存在的离子平衡,能举例说明离子反应与平衡在生产、生活中的应用
1.弱电解质(1)概念(2)与化合物类型的关系强电解质主要是大部分离子化合物及某些共价化合物,弱电解质主要是某些共价化合物
2.弱电解质的电离概念(1)电离平衡的建立在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率相等时,电离过程达到了平衡
(2)电离平衡的建立与特征①开始时,v(电离)最大,而v(结合)为0
②平衡的建立过程中,v(电离)>v(结合)
③当v(电离)=v(结合)时,电离过程达到平衡状态
3.外因对电离平衡的影响(1)浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离
(2)温度:温度越高,电离程度越大
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方向移动
(4)化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移动
理解应用以0
1mol·L-1CH3COOH溶液为例,填写外界条件对CH3COOHCH3COO-+H+ΔH>0的影响
改变条件平衡移动方向n(H+)c(H+)导电能力Ka加水稀释向右增大减小减弱不变加入少量冰醋酸向右增大增大增强不变通入HCl(g)向左增大增大增强不变加NaOH(s)向右减小减小增强不变加CH3COONa(s)向左减小减小增强不变加入镁粉向右减小减小增强不变升高温度向右增大增大增强增大4
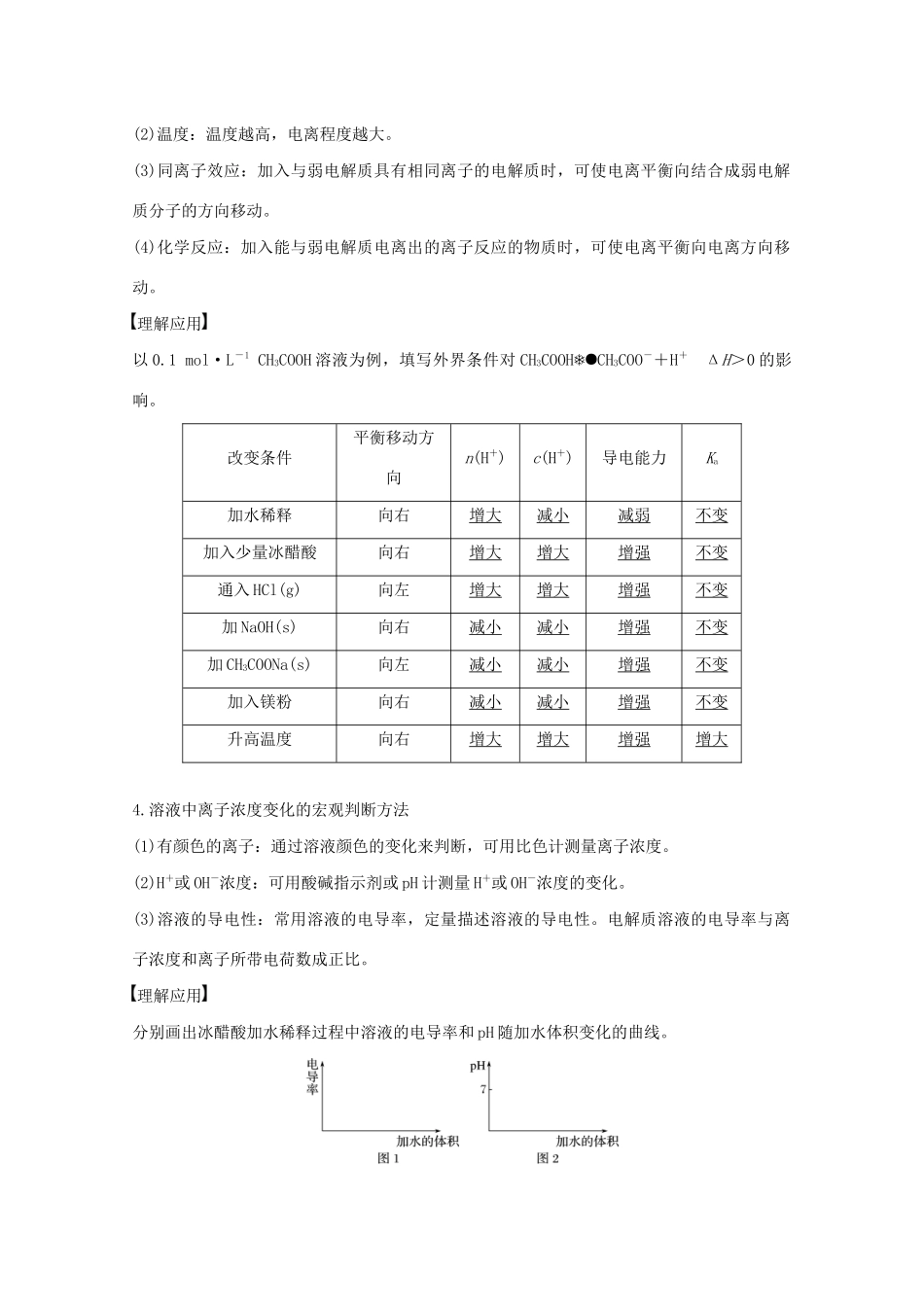
溶液中离子浓度变化的宏观判断方法(1)有颜色的离子:通过溶液颜色的变化来判断,可用比色计测量离子浓度